검색결과 리스트
바이오종목/Helixmith(바이로메드)에 해당되는 글 275건
- 2019.05.18 `유전자·세포치료제` 이미 트렌드‥생산방법·비싼비용 고민`ASGCT`에서 확인한 유전자·세포치료제 방향성‥몇년 사이 급증가한 연구 눈길
- 2019.05.06 유상증자 관련 소문에 대한 개인적인 생각
- 2019.04.29 Genopis 인력 채용 관련
- 2019.04.29 약업닷컴 홈 > 글로벌뉴스 > 전체美 제약업계, 167개 당뇨병 치료제 개발 매진PhRMA 보고서, 1형 32개‧2형 77개‧관련 치료제 68개 등
- 2019.04.26 Thrombocytopenia Treatment Market Trends and Growth 2026: Top Players STATegics, Inc., and ViroMed Co., Ltd.
- 2019.04.12 '안 아파서' 무서운 당뇨발…작은 상처에도 다리절단
- 2019.04.05 주식등의 대량보유상황보고서
- 2019.04.04 "레일라 영광 다시한번"…피엠지-바이로메드 공동연구
- 2019.04.03 R&D투자 늘린 바이오제약..제일·SK바이오팜 50%↑
- 2019.04.02 VM-202 간헐성 파행증
글
`유전자·세포치료제` 이미 트렌드‥생산방법·비싼비용 고민`ASGCT`에서 확인한 유전자·세포치료제 방향성‥몇년 사이 급증가한 연구 눈길
설정
트랙백
댓글
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| "2017년 7월 인보사 허가엔 문제없었다" (0) | 2019.05.21 |
|---|---|
| Effective control of neuropathic pain by hepatocyte growth factor transiently expressed from naked plasmid DNA 플라스미드 DNA에 의해 일시적으로 발현되는 간세포 성장인자에 의한 효과적 신경병성 통증 조절 (0) | 2019.05.18 |
| 유상증자 관련 소문에 대한 개인적인 생각 (0) | 2019.05.06 |
| Genopis 인력 채용 관련 (0) | 2019.04.29 |
| 약업닷컴 홈 > 글로벌뉴스 > 전체美 제약업계, 167개 당뇨병 치료제 개발 매진PhRMA 보고서, 1형 32개‧2형 77개‧관련 치료제 68개 등 (0) | 2019.04.29 |
글
네이버 카페에 유상증자 관련 소문으로 주말 연휴에 주주 여러분들 모두 불안하고 힘들게 보내고 계시는 군요.
투자는 개인의 책임이며 여유자금이 아닌 이상 모두 안 좋은 뉴스에 민감하게 반응하고 걱정들이 많은 것 같습니다.
이번 기회에 본인의 투자 가치관은 여유롭고 안정적인지 다시 고민해 보시기 바랍니다.
저는 개인적으로 일단 회사를 믿고 기다려 볼려고 합니다. 뭐 고민해 봐도 별다른 방법은 없는 것 같습니다.
1-2년 전부터 바이로메드가 미국에서 능력있는 박사님들 채용하고 그 분들 스탁옵션도 받고 또 미국 fda에서 오랫동안 근무하신 분도 모셔오고, 미국 제노피스 생산시설 인수, 세계적인 컨설팅 회사에 근무하시던 젊은 이사님들도 모셔오고 회사는 성장을 이어가고 있지만 회사 향후 자금에 대한 불안은 항상 마음 한구석에 자리잡고 있습니다.
어떻게 하겠습니까 ? 회사에 안정적인 매출 또는 LO 등으로 큰 자금이 들어 오지 않는 이상 작은 바이오 회사는 자금 압박에 시달릴 수 밖에요... 미국 임상 3상, 생산시설 인수 및 운영, 마곡 사옥 공사 및 완공에도 엄청나게 많은 자금이 필요합니다.
저는 기다려 볼려고 합니다. 저희 개미 투자자들 보다 그리고 공매도 치는 기관보다 작년부터 계속 매수하는 세계적인 펀드 회사 그리고 무엇보다 대주주인 김선영 박사님의 지분 매도 소식은 없습니다. 또한 미국 및 한국 우수한 직원들이 저희들보다는 바이로메드가 개발하고 있는 신약에 대해서 더 잘알고 있을 것으로 판단됩니다.
그럼 모두 성공적인 투자를 기원드립니다.
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
글
https://www.indeed.com/q-Quality-Assurance-Manager-l-San-Diego,-CA-jobs.html?vjk=dc669e3d76bf1ef0
Quality Assurance Manager Jobs, Employment in San Diego, CA | Indeed.com
Quality Assurance Manager jobs in San Diego, CA Filter results by: Sort by: relevance - date San Diego, CA (437) Chula Vista, CA (15) La Jolla, CA (7) Poway, CA (7) El Cajon, CA (6) Jamul, CA (4) Encinitas, CA (3) Coronado, CA (3) National City, CA (2) Del
www.indeed.com
유전자 치료제 생산과 FDA 승인을 위해 작년부터 전문 인력을 계속 채용하고 있습니다.
미국 임상 3상 결과에 대한 자신감이 이런곳에서 보여주는 군요... 조만간 좋은 소식을 기대해 봅니다.
회사의 가치는 계속 성장하고 있습니다. 주가의 변동성은 신경 쓰면 쓸수록 스트레스만 많아집니다.
회사를 믿고 그 회사의 기술력과 향후 상용화시에 시장에 미치는 영향을 고민하시기 바랍니다.
주가가 하락하면 힘들지만 끈기와 인내로 이겨내어야 달콤한 결과를 얻을 수 있을 것입니다.
Manager/Sr Manager Quality Assurance, GCP
Genopis Inc - San Diego, CA 92121
$110,000 - $115,000 a year
Summary
The Manager/Sr. Manager of GcP Quality Assurance evaluates, maintains and enhances Quality Compliance activities to ensure that ViroMed Quality and Compliance Standards and applicable Government Regulations are met, and vendors achieve, maintain and improve the current level of compliance.
Responsibilities
-
Facilitates the development, implementation and maintenance of QA systems and SOPs for GCP activities.
-
Supports daily and end-to-end compliance aspects of the portfolio of GcP focused vendors in a virtual work environment.
-
Works with internal GcP customers and develop and execute strategic audit plans.
-
Coordinates, develops, maintains and/or provides GcP training.
-
Maintains relevant knowledge of both local and international auditing and appropriate GcP requirements and developments as they impact ViroMed SOPs and compliance with GcP, and communicate these to QA management, as applicable.
-
Provides extensive experience in quality assurance, regulatory affairs, auditing, clinical research, monitoring, data management, pharmacy, laboratory, or other relevant areas, including applicable GcP auditing.
-
Provides expertise in GcP regulations and guidance for FDA and International agencies including ICH guidelines.
-
Stays current with industry best practices and regulatory guidance.
-
Plans, prepares, performs and reviews audits according to the audit schedule.
-
Trending QMS and audit findings
-
Reviews clinical deviations and clinical deviation trends.
-
Ensures the establishment of an appropriate audit responses and timescale of corrective actions in cooperation with vendors/stakeholders
-
Monitors vendor corrective and preventive actions.
-
Supports the Internal Audit Program.
-
Participates in Inspection Readiness activities including FDA "Mock" inspections, training and support activities.
-
Supports Regulatory and Third-Party Inspections.
-
Ensures Risk Registrars are prepared and maintained for clinical studies and Drug Program issues.
-
Other GcP related tasks, as assigned.
Requirements
Professional Experience/ Qualifications
BA/BS in science or equivalent with at least 5-8 years relevant experience in the Pharmaceutical Industry
-
In-depth knowledge of Pharmaceutical regulations: GcP, PV, and Health regulations (ICH, FDA, EU, main local regulations).
-
In-depth knowledge of Pharmaceutical Operations
-
Thorough experience auditing GcP regulated areas
-
Experience in FDA Regulatory Inspection supportㅍ
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| `유전자·세포치료제` 이미 트렌드‥생산방법·비싼비용 고민`ASGCT`에서 확인한 유전자·세포치료제 방향성‥몇년 사이 급증가한 연구 눈길 (0) | 2019.05.18 |
|---|---|
| 유상증자 관련 소문에 대한 개인적인 생각 (0) | 2019.05.06 |
| 약업닷컴 홈 > 글로벌뉴스 > 전체美 제약업계, 167개 당뇨병 치료제 개발 매진PhRMA 보고서, 1형 32개‧2형 77개‧관련 치료제 68개 등 (0) | 2019.04.29 |
| Thrombocytopenia Treatment Market Trends and Growth 2026: Top Players STATegics, Inc., and ViroMed Co., Ltd. (0) | 2019.04.26 |
| '안 아파서' 무서운 당뇨발…작은 상처에도 다리절단 (0) | 2019.04.12 |
글
약업닷컴 홈 > 글로벌뉴스 > 전체美 제약업계, 167개 당뇨병 치료제 개발 매진PhRMA 보고서, 1형 32개‧2형 77개‧관련 치료제 68개 등
설정
트랙백
댓글
http://www.yakup.com/news/index.html?mode=view&cat=16&nid=229876
[약업신문]美 제약업계, 167개 당뇨병 치료제 개발 매진
현재 미국 내 당뇨병 환자 수는 진단을 받지 못한 720만명을 포함해 총 3,000만명을 상회할 것으로 추정되고 있다. 또한 매년 150만명에 육박하는 새로운 환자들이 매년 당뇨병 발병을 진단받고 있는 추세여서...
www.yakup.com
미국 내 당뇨병 환자 수 3,000만명...
바이로메드의 VM-202 DPN, PAD는 시장성이 무궁무진합니다.
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| 유상증자 관련 소문에 대한 개인적인 생각 (0) | 2019.05.06 |
|---|---|
| Genopis 인력 채용 관련 (0) | 2019.04.29 |
| Thrombocytopenia Treatment Market Trends and Growth 2026: Top Players STATegics, Inc., and ViroMed Co., Ltd. (0) | 2019.04.26 |
| '안 아파서' 무서운 당뇨발…작은 상처에도 다리절단 (0) | 2019.04.12 |
| 주식등의 대량보유상황보고서 (0) | 2019.04.05 |
글
Thrombocytopenia Treatment Market Trends and Growth 2026: Top Players STATegics, Inc., and ViroMed Co., Ltd.
설정
트랙백
댓글
Thrombocytopenia Treatment Market Trends and Growth 2026: Top Players STATegics, Inc., and ViroMed Co., Ltd. - Business Herald
Thrombocytopenia is a disorder in which a patient has low level of platelets in the blood.
businessherald.co
혈소판 감소증에도 바이로메드는 Top Player 입니다.
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| Genopis 인력 채용 관련 (0) | 2019.04.29 |
|---|---|
| 약업닷컴 홈 > 글로벌뉴스 > 전체美 제약업계, 167개 당뇨병 치료제 개발 매진PhRMA 보고서, 1형 32개‧2형 77개‧관련 치료제 68개 등 (0) | 2019.04.29 |
| '안 아파서' 무서운 당뇨발…작은 상처에도 다리절단 (0) | 2019.04.12 |
| 주식등의 대량보유상황보고서 (0) | 2019.04.05 |
| "레일라 영광 다시한번"…피엠지-바이로메드 공동연구 (0) | 2019.04.04 |
글
http://news.mt.co.kr/mtview.php?no=2019041019334420145&MTS_P
'안 아파서' 무서운 당뇨발…작은 상처에도 다리절단 - 머니투데이 뉴스
'연중기획-메디슈머(Medical+Consumer) 시대'는 코스피상장사 메디파트너생명공학과 함께 합니다.#1. 당뇨병 환자인 A씨(46)는 맨발로 화장실 청소를 했다가 한 달여 만에 종아리 부분을 ...
news.mt.co.kr
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| 약업닷컴 홈 > 글로벌뉴스 > 전체美 제약업계, 167개 당뇨병 치료제 개발 매진PhRMA 보고서, 1형 32개‧2형 77개‧관련 치료제 68개 등 (0) | 2019.04.29 |
|---|---|
| Thrombocytopenia Treatment Market Trends and Growth 2026: Top Players STATegics, Inc., and ViroMed Co., Ltd. (0) | 2019.04.26 |
| 주식등의 대량보유상황보고서 (0) | 2019.04.05 |
| "레일라 영광 다시한번"…피엠지-바이로메드 공동연구 (0) | 2019.04.04 |
| R&D투자 늘린 바이오제약..제일·SK바이오팜 50%↑ (0) | 2019.04.03 |
글
http://dart.fss.or.kr/dsaf001/main.do?rcpNo=20190405001976
바이로메드/주식등의대량보유상황보고서(일반)/2019.04.05
dart.fss.or.kr
김선영 대표이사 주식 담보 대출 약 300억 정도...
작년 1,000억 cb 발행할때 30% 콜옵션과 관련이 있는 것 같기도 한데.. 자세한 내용은 아직 모르겠네요..
[Call Option에 관한 사항]
가. 제3자의 성명 : 발행일 현재 미정
나. 제3자와 회사와의 관계 : 최대주주, 특수관계자 및 임직원
다. 취득규모 : 최대 300억원 (Call Option 30%)
라. 취득목적 : 안정적인 경영권 확보 및 투자자 이익보호
마. 제3자가 될 수 있는 자 : 최대주주, 특수관계자 및 임직원
바. 제3자가 얻게 될 경제적 이익 : 제3자가 될 수 있는 자가 콜옵션을 통하여 취득한 전환사채로 전환권을 행사할 경우 최초 전환가액 기준 당사 보통주 123,474주를 취득할 수 있게 되며, 리픽싱 85% 조정 후에는 최대 145,264주까지 취득 가능함. 이에 제3자가 될 수 있는 자는 당사 지분율을 0.75%에서 최대 0.88%(리픽싱 85%)까지 보유 가능. 이 경우 전환으로 인한 이익은 행사시점의 주가 수준에 따라 달라질 수 있음.
============================================================================
가. 계약 여부
| 신탁ㆍ담보ㆍ대차ㆍ일임ㆍ장외매매ㆍ공동보유 등 주요계약 체결, 변경 여부 |
| 있음 |
*주요계약 체결ㆍ변경사실 미보고시 해당 미보고분에 대해 의결권이 제한될 수 있음
나. 계약 내용
성명(명칭)보고자와의관계생년월일 또는사업자등록번호 등주식등의종류주식등의수계약 상대방계약의종류계약체결(변경)일계약기간비율비고
| 김선영 | 본인 | 551103 | 의결권있는 주식 | 44,417 | 신한금융투자 | 담보계약 | 2017년 12월 01일 | 2019년9월30일 | 0.28 | 주식담보대출 |
| 김선영 | 본인 | 551103 | 의결권있는 주식 | 85,061 | 신한금융투자 | 담보계약 | 2019년 04월 01일 | 2019년9월30일 | 0.53 | 주식담보대출 |
| 합계(주식등의 수) | 129,478 | 합계(비율) | 0.81 | - | ||||||
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| Thrombocytopenia Treatment Market Trends and Growth 2026: Top Players STATegics, Inc., and ViroMed Co., Ltd. (0) | 2019.04.26 |
|---|---|
| '안 아파서' 무서운 당뇨발…작은 상처에도 다리절단 (0) | 2019.04.12 |
| "레일라 영광 다시한번"…피엠지-바이로메드 공동연구 (0) | 2019.04.04 |
| R&D투자 늘린 바이오제약..제일·SK바이오팜 50%↑ (0) | 2019.04.03 |
| VM-202 간헐성 파행증 (0) | 2019.04.02 |
글
http://www.dailypharm.com/Users/News/NewsView.html?ID=251178
레일라 영광 다시한번…피엠지-바이로메드 공동연구
한국피엠지제약이 바이로메드와 새로운 관절염치료제를 공동개발하기로 했다. 양사는 이전에 천연물신약 레일라정을 공동개발해 관절염치료제 시장에서 블록버스터로 성장시킨 바 있다. 한국피엠지제약(대표 전영진)은 지난달 21일 바이오벤처 바이로메드와 새로운 관절염 치료제 공동개발에 대한 연구계약을 체결했다고 밝혔다. 피엠지는 바이로메드로부터 해당 약물의 기술을 제공받아 임상시험을 통해 제품을 상업화...
www.dailypharm.com
한국피엠지제약이 바이로메드와 새로운 관절염치료제를 공동개발하기로 했다. 양사는 이전에 천연물신약 '레일라정'을 공동개발해 관절염치료제 시장에서 블록버스터로 성장시킨 바 있다.
한국피엠지제약(대표 전영진)은 지난달 21일 바이오벤처 '바이로메드'와 새로운 관절염 치료제 공동개발에 대한 연구계약을 체결했다고 밝혔다.
피엠지는 바이로메드로부터 해당 약물의 기술을 제공받아 임상시험을 통해 제품을 상업화할 계획이다. 연간 200억원 가량 매출을 올리고 있는 레일라정도 피엠지가 바이로메드로부터 기술이전을 받아 2012년 출시했다.
양사가 이번에도 협력을 통해 관절염치료제 분야에서 새로운 블록버스터를 만들어낼지 주목된다.
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| '안 아파서' 무서운 당뇨발…작은 상처에도 다리절단 (0) | 2019.04.12 |
|---|---|
| 주식등의 대량보유상황보고서 (0) | 2019.04.05 |
| R&D투자 늘린 바이오제약..제일·SK바이오팜 50%↑ (0) | 2019.04.03 |
| VM-202 간헐성 파행증 (0) | 2019.04.02 |
| 상호변경안내 (0) | 2019.03.28 |
글
http://biospectator.com/view/news_view.php?varAtcId=7396
R&D투자 늘린 바이오제약..제일·SK바이오팜 50%↑
제일약품, SK바이오팜, 일양약품, 코오롱생명과학이 지난해 연구개발(R&D) 투자를 50% 이상 늘린 것으로 나타났다. 가장 많은 R&D 비용을 집행한 바이
www.biospectator.com
==============================
국내 바이오제약 2018년 사업보고서 분석..R&D 규모는 셀트리온·한미약품·삼성바이오에피스·GC녹십자순
제일약품, SK바이오팜, 일양약품, 코오롱생명과학이 지난해 연구개발(R&D) 투자를 50% 이상 늘린 것으로 나타났다. 가장 많은 R&D 비용을 집행한 바이오제약기업은 셀트리온, 한미약품, 삼성바이오에피스, GC녹십자순이었다.
3일 바이오스펙테이터가 2018년 사업보고서를 바탕으로 200억원 이상의 R&D투자를 한 국내 바이오제약기업을 분석한 결과 총 23곳이 1조7786억원을 투자한 것으로 나타났다.
이는 전년 1조6217억원 대비 9.7%가 증가한 것으로 국내 바이오제약기업들이 어려운 경영환경에도 불구하고 미래성장 동력을 찾기 위해 적극적인 투자를 집행했다.
23곳 중에서는 한미약품 GC녹십자 대웅제약 등 제약사가 16곳을 차지했지만 셀트리온, SK바이오팜, 신라젠과 같은 신약개발기업(바이오시밀러 포함) 7곳도 이름을 올렸다.
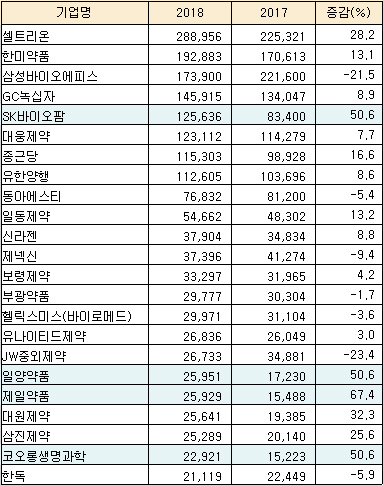
가장 많은 R&D비용을 집행한 곳은 셀트리온으로 전년보다 28.2%를 늘린 2889억5600만원으로 투자했다. 유일한 2000억원대 투자기업이기도 하다.
한미약품도 13.1% 증가한 1928억8300만원을 투자했다. 이어 삼성바이오에피스(1739억원), GC녹십자(1459억1500만원), SK바이오팜(1256억3600만원) 등의 순으로 총 7곳이 1000억원대 투자기업이었다.
23곳 중 16곳이 R&D비용을 늘렸다. 이중 제일약품은 가장 높은 증가율(67.4%, 259억2900만원)을 보였고 이어 SK바이오팜 1256억3600만원(50.6%), 일양약품 259억5100만원(50.6%), 코오롱생명과학 229억2100만원(50.6%)이 나란히 50% 이상의 증가율을 기록했다.
국내 바이오텍인 신라젠, 제넥신, 헬릭스미스(바이로메드) 등도 각각 379억400만원, 373억9600만원, 299억7100만원의 R&D 비용을 투자했다. 국내 바이오산업이 주목받으면서 자체적인 매출은 적지만 적극적인 외부투자로 인해 공격적인 R&D를 집행할 수 있었다는 분석이다. 제넥신은 지난해 2500억원, 헬릭스미스는 1000억원 규모의 투자를 유치했다.
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| 주식등의 대량보유상황보고서 (0) | 2019.04.05 |
|---|---|
| "레일라 영광 다시한번"…피엠지-바이로메드 공동연구 (0) | 2019.04.04 |
| VM-202 간헐성 파행증 (0) | 2019.04.02 |
| 상호변경안내 (0) | 2019.03.28 |
| 바이로메드 "미국 임상 개발 위한 6가지 성공 조건" (0) | 2019.03.28 |
글
https://blog.naver.com/hyosuby2005/221502872594
VM202-Claudication
이번 주총에서 언급된 내용 중, 관심있게 본 것 중 하나가 claudication 입니다.Intermittent claudicatio...
blog.naver.com
필사즉생님의 블로그에 아주 좋은 글이 올라와서 공유합니다.
'바이오종목 > Helixmith(바이로메드)' 카테고리의 다른 글
| "레일라 영광 다시한번"…피엠지-바이로메드 공동연구 (0) | 2019.04.04 |
|---|---|
| R&D투자 늘린 바이오제약..제일·SK바이오팜 50%↑ (0) | 2019.04.03 |
| 상호변경안내 (0) | 2019.03.28 |
| 바이로메드 "미국 임상 개발 위한 6가지 성공 조건" (0) | 2019.03.28 |
| DPN 임상 3상 결과 발표 , 2019년 8월 (0) | 2019.03.27 |


RECENT COMMENT