검색결과 리스트
바이오종목/강스템바이오텍에 해당되는 글 81건
- 2019.02.28 두필루맙, 새로운 천식 치료제로 자리매김할까
- 2019.02.28 내달 지수 변경..."코스피-중형주·코스닥-대형주 노려라"
- 2019.02.28 강스템바이오텍 2019년도 상반기 인력 채용
- 2019.02.27 강스템바이오텍 - 제대혈 줄기세포기반 신약Pipeline 임상중·목표가 미제시
- 2019.02.25 거부반응 없는 '만능줄기세포' 세계 첫 개발 美샌프란시스코 UC 연구팀 보고, 줄기세포 유전자편집 '돌파구'
- 2019.02.23 제대혈 줄기세포 기반 신약Pipeline 임상 중
- 2019.02.23 아토피 피부염 경쟁사 사노피의 Dupilumab 관련 내용
- 2019.02.22 강스템바이오텍, '줄기세포 GMP 센터' 4월 완공…3.6만 바이알로 확대
- 2019.02.22 강 경 선 교수 서울대학교 수의과대학 성체줄기연구센터
- 2019.02.21 IR ROOM 질문과 답변
글
http://www.monews.co.kr/news/articleView.html?idxno=201087
듀피루맙이 천식에도 효과가 있다는 뉴스..
강스템에서 개발한 Furestem AD주도 천식에 효과가 있겠다는 생각이 드네요...
원리는 똑 같으니까....
======================================================================
AAAAI 2019] 알레르기 비염, 아토피 피부염, 만성 비부비동염 동반한 천식 환자에 효과
강제호기량, 중증 악화율, 염증 수치 등 개선
[메디칼업저버 최상관 기자] 두필루맙(제품명 듀피젠트)이 여러 질환을 동반한 천식 환자에 대해 효과를 대거 입증하면서 차후 행보가 주목되고 있다.
22일~25일 미국 샌프란시스코에서 열린 미국알레르기·천식면역학회(AAAAI) 학술대회에서 발표된 두필루맙 관련 연구에 따르면, 두필루맙은 알레르기 비염, 아토피 피부염, 만성 비부비동염 등을 동반한 천식 환자에게도 효과를 입증한 것으로 나타났다.
두필루맙은 인터루킨(IL)-4 수용체 길항제로 IL-4와 IL-13 경로에 관여하는 단일클론 항체 치료제다. 처음에는 습진이나 피부염 등 알레르기 질환 치료제로 등장했다.
이후 두필루맙은 지난해 10월 미국식품의약국(FDA)로부터 추가 적응증을 획득하면서, 호산구 표현형(phenotype) 또는 경구용 코르티코스테로이드 의존성 천식을 동반한 12세 이상 중등도~중증 천식 환자에게도 사용할 수 있게 됐다.
이번 학술대회에서 발표된 연구를 통해 두필루맙은 더 다양한 유형의 천식 환자에게 적용될 가능성을 높였다.
알레르기 비염 동반 천식 환자에 효과 입증
알레르기 비염을 동반한 천식에 대한 효과는 LIBERTY ASTHMA QUEST 임상3상 연구를 사후 분석(post hoc analysis)한 결과를 통해 확인됐다(Abstract #293).
연구에는 알레르기 비염을 동반하면서 천식 조절에 어려움을 겪는 중증 천식 환자를 두필루맙 200mg 또는 300mg 투여군 위약군에 각각 배정해 치료 효과를 평가했다. 약제는 2주 간격으로 투여했으며, 효과는 1초 강제호기량(FEV₁) 및 연간 중증 악화율의 변화를 통해 평가했다.
그 결과 알레르기 비염을 동반한 천식 환자에게도 두필루맙의 치료 효과가 우수했다.
두필루맙 200mg 투여군 중 알레르기 비염 동반 또는 동반하지 않은 환자는 위약보다 중증 악화 위험이 각각 40%(RR 0.606; 95% CI; 0.451-0.814 P=0.0009), 60%가량 낮았다(0.406; 0.273-0.605; P<0.0001). 이는 300mg 투여군에서도 유사한 결과를 보였다.
또한 두필루맙 200mg 투여군 중 위약대비 12주간 FEV₁ 개선율은 알레르기 비염 동반 환자가 0.14L(95% CI 0.07-0.21; P<0.0001). 알레르기 비염을 동반하지 않은 환자는 0.13L 개선된 것으로 나타났다(95% CI 0.05-0.22; P<0.0023). 이러한 효과는 52주간 지속됐으며 300mg 투여군에서도 유사했다.
또한 두필루맙은 천식 환자에서 증가하는 호기산화질소(FeNO)를 비롯한 면역글로불린E(IgE), 이오탁신(eotaxin) 등 염증 바이오마커 수치도 위약 대비 유의미하게 감소시켰다(abstract #294).
아울러 두필루맙은 위약 대비 알레르기 비염을 동반한 중등도~중증 천식 환자의 삶의 질도 유의하게 개선했다. 이는 '비염 관련 삶의 질 설문지(Rhinoconjunctivitis Quality of Life Questionnaire, RQLQ)'를 통해 환자의 삶의 질을 평가한 결과다(abstract #304).
두필루맙군에서 나타난 가장 흔한 이상반응은 주사부위 부작용으로 200mg군과 300mg군의 부작용 발생률은 각각 15%, 18%였으나 위약군은 5%, 10%에 그쳤다.
연구에 참여한 미국 위스콘신의대 William W. Busse 교수는 "두필루맙은 알레르기 비염 동반 여부와 상관없이 천식 조절이 어려움을 겪는 중증 환자에게 유의한 효과를 보였다"고 밝혔다.
천식, 아토피 피부염, 만성 비부비동염 모두 개선
두필루맙은 천식, 아토피 피부염, 만성 비부비동염을 모두 동반한 환자에 대해서도 효과를 입증했다(Abstract #370).
이는 미국 콜로라도의대 Mark Boguniewicz 교수팀이 임상3상 연구 네 건 LIBERTY AD SOLO 1 & 2, CHRONOS, CAFE 등을 분석한 결과다.
분석에 포함된 환자는 두필루맙(300mg) 2주마다 투여군, 매주 투여군, 위약군으로 분류됐다.
이후 치료 16주째 천식, 만성 비부비동염, 아토피 피부염 등의 예후를 평가했다. 평가는 각각 천식관리설문(ACQ-5), 비부비동염 특이 설문(SNOT-22), 습진 범위 및 중증도 지수(EASI), 최대 소양증 등급평가(pp-NRS) 등을 통해 이뤄졌다.
그 결과 두필루맙을 2주마다 또는 매주 투여군은 ACQ-5 점수가 각각 평균 0.53점, 0.66점 개선됐으나 위약군은 0.24점 개선되는 데 그쳤다. SNOT-22 점수도 두필루맙군은 각각 12.27점, 13.39점 개선됐으나 위약군은 6.47점에 그쳤다. 또한 두필루맙군의 EASI 개선율은 각각 77.7%, 75.3%로 위약군(35.5%)보다 더 우월했고, pp-NRS 개선율도 각각 46.1%, 50.7%로 위약군(24%)보다 더 나은 모습을 보였다.
Boguniewicz 교수는 "이번 하위 그룹 분석을 통해 두필루맙이 천식, 아토피 피부염, 만성 비부비동염을 모두 동반한 환자에 임상적, 통계적으로 의미있는 치료 효과를 보이는 것으로 나타났다"고 말했다.
연구에 참여한 벨기에 겐트의대 Claus Bachert 교수는 "두필루맙은 제2형 염증성 질환을 치료하는 핵심 열쇠"라며 "지금까지 치료에 어려움을 겪었던 만성 비부비동염을 동반한 천식 환자는 두필루맙을 통해 치료의 새 전환기를 마련할 수 있게 됐다"고 평가했다.
출처 : 메디칼업저버(http://www.monews.co.kr)
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 제약바이오협회, ‘KPBMA 바이오 오픈 플라자’ 개최 (0) | 2019.03.12 |
|---|---|
| [CEO리포트]서명관 강스템 부사장 "美 JP모건서 아토피신약 깊은 관심 보여" (0) | 2019.03.03 |
| 내달 지수 변경..."코스피-중형주·코스닥-대형주 노려라" (0) | 2019.02.28 |
| 강스템바이오텍 2019년도 상반기 인력 채용 (0) | 2019.02.28 |
| 강스템바이오텍 - 제대혈 줄기세포기반 신약Pipeline 임상중·목표가 미제시 (0) | 2019.02.27 |
글
https://news.naver.com/main/read.nhn?mode=LSD&mid=sec&oid=011&aid=0003512633&sid1=001
3월달부터는 코스닥100에 강스템바이오텍이 편입되니 자연스럽게 기관들의 매수세가 이어질 전망...
대형 뉴스 한 두개 씩 나오면 주가는 계속 우상향 할 것임.
직원들도 계속 채용하고 있고 해외 진출도 가시화 되고 있음. 무엇보다 아토피 치료제 국내 임상 3상 결과만 좋게 나오면 2020년 부터는 의미있는 본격적인 상용화 매출이 본격화 될 것임.
그럼 이 회사는 앞으로 크게 걱정 안해도 성장 할 것임. 왜 ? 직원들 수도 별로 많지 않고 생산 공장 확장하는데 큰 돈 안들어가고 무엇보다 줄기세포 치료제 특허로 10년 간은 경쟁사 없음.
해외 아토피 시장 진출과 다른 파이프라인 임상 결과만 좋게 나오면 이 회사 주식은 10년 이상 보유해야 할 것임.
==================================================================
코스피선 LG이노텍 등 35곳 편입
코스닥은 카페24 등 25곳 진입
[서울경제] 매년 1회 진행되는 3월 시가총액 규모별 지수의 정기변경을 앞두고 투자자들의 관심이 높아지는 가운데 코스피의 경우 중형주, 코스닥은 대형주에 새로 편입되는 종목에 주목해야 한다는 조언이 나왔다.
한국거래소는 매년 3월 선물·옵션 동시 만기일의 다음날(3월15일) 코스피·코스닥 모두 대형·중형·소형주 3개 지수에 각각 새로 편입되거나 빠지는 종목을 발표한다. 규모별 지수에 대한 국내 기관투자가의 선호도가 높은 만큼 관련 종목들의 주가가 출렁인다.
27일 금융투자업계에 따르면 코스피의 경우 중형주 신규 편입 종목에 수급이 몰릴 가능성이 제기됐다. 이중호 KB증권 연구원은 “대형주에 우량주가 더 많지만 코스피200·KRX300 등 대안이 많아 코스피 대형주 지수는 상대적으로 주목을 덜 받는다”며 “반면 중형주는 중형주 지수 외에는 대안이 없어 투자가 집중될 수밖에 없는 구조”라고 설명했다. KB증권에 따르면 최근 5년 동안 중형주 지수의 평균수익률은 코스피 평균 수익률을 최대 12.9% 초과했다.
현재 LG이노텍(011070)과 동서(026960)·녹십자(006280)·한샘(009240)·만도(204320)·HDC(012630)·효성(004800)(이상 대형주), HDC산업개발·애경산업(018250)(미분류) 등 35개 종목이 새로 코스피 중형주에 이름을 올릴 것으로 예상된다.
코스닥에서는 우량 대형주를 모아둔 코스닥100에 새로 들어서는 종목에 관심을 기울일 필요가 있다. 전균 삼성증권 연구원은 “특히 코스닥100과 많은 종목이 겹치며 코스닥 벤치마크 지수로 많이 활용되는 코스닥150은 현재 지수선물과 ETF가 상장돼 있어 정기변경에 다른 수급 변화가 활발하다”고 말했다. 국민연금의 국내주식 벤치마크에는 ‘위탁’ 부분에 코스닥100이 포함돼 있기도 하다.
코스닥100에는 세계적인 투자가인 짐 로저스를 사외이사로 선임한 경협주 아난티(025980)를 비롯해 카페24(042000)·아프리카TV(067160)·RFHIC(218410) 등 정보기술(IT)·통신주, 안트로젠(065660)·에이치엘비생명과학(067630)·엔지켐생명과학(183490)·강스템바이오텍 등 바이오주 등 총 25개 종목이 새로 편입될 예정이다. 전 연구원은 “지난해 33종목의 신규 편입 이후 평균 수익률은 같은 기간 코스닥보다 10% 높았다”며 “지난해 코스닥이 유례없는 부진을 겪은 점을 고려해도 높은 수익률”이라고 설명했다.
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| [CEO리포트]서명관 강스템 부사장 "美 JP모건서 아토피신약 깊은 관심 보여" (0) | 2019.03.03 |
|---|---|
| 두필루맙, 새로운 천식 치료제로 자리매김할까 (0) | 2019.02.28 |
| 강스템바이오텍 2019년도 상반기 인력 채용 (0) | 2019.02.28 |
| 강스템바이오텍 - 제대혈 줄기세포기반 신약Pipeline 임상중·목표가 미제시 (0) | 2019.02.27 |
| 거부반응 없는 '만능줄기세포' 세계 첫 개발 美샌프란시스코 UC 연구팀 보고, 줄기세포 유전자편집 '돌파구' (0) | 2019.02.25 |
글
1. 해외 라이센싱 관련 경력 직원 모집
2. 줄기세포 제조 및 품질 관리 : 신입 / 경력 / 영어 능통자...
저의 개인적인 판단은 해외 진출을 목적으로 인력 채용하는 것입니다.
강스템 바이오텍 현재 인력이 85명 인데 이렇게 다양한 분야에 인력을 한번에 충원하는 것은 회사가 더 큰 회사로 성장하겠다는 것입니다.
그냥 주식 매수해두고 급락하면 더 매수해서 물량 잘 챙겨놓으시기 바랍니다.
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 두필루맙, 새로운 천식 치료제로 자리매김할까 (0) | 2019.02.28 |
|---|---|
| 내달 지수 변경..."코스피-중형주·코스닥-대형주 노려라" (0) | 2019.02.28 |
| 강스템바이오텍 - 제대혈 줄기세포기반 신약Pipeline 임상중·목표가 미제시 (0) | 2019.02.27 |
| 거부반응 없는 '만능줄기세포' 세계 첫 개발 美샌프란시스코 UC 연구팀 보고, 줄기세포 유전자편집 '돌파구' (0) | 2019.02.25 |
| 제대혈 줄기세포 기반 신약Pipeline 임상 중 (0) | 2019.02.23 |
글
http://betanews.heraldcorp.com:8080/article/979820.html
2020년이 기대되는 종목은 강스템바이오텍...
2020년에 매수 하고 싶지만 이 종목은 언제 상승해 버릴지 모르니 저렴할때 최대한 물량 확보해야 함. !
===========================================================
강스템바이오텍( 코스닥 217730)은 줄기세포치료제를 전문으로 하는 바이오 제약사로 2010년 설립후 줄기세포치료제를 집중적으로 연구개발해왔다. 주요사업은 다분화특성을 가진 줄기세포를 인간 제대혈로부터 분리 대량배양하는 기술을 기반으로 한 동종제대혈 유래 줄기세포치료제 연구개발이다. 주요제품은 퓨어스템 에이디 퓨어스템 알에이 등이 있다. 정부에서 지원하는 크론병 중개연구센터 컨소시엄에 참여하는 유일한 기업체로서 서울아산병원 삼성서울병원 등 국내 주요 종합병원들과 긴밀한 네트워크를 구축하고 있다. 또한 제약사와의 협력으로 경쟁력을 강화하고 있다. 제대혈 줄기세포를 이용하여 아토피피부염과 크론병 류마티스관절염 등 희귀 난치성면역질환 치료제 개발업체로 2015년 기술성장특례제도를 통해 코스닥 시장에 상장했다.
자체 개발한 다분화 줄기세포를 인간제대혈로부터 고순도로 분리하여 대량배양하는 기술을 바탕으로 동종제대혈 유래줄기세포치료제 연구개발을 주요 사업으로 펼쳐가고 있다. 아토피 피부염에 대응한 줄기세포치료제의 상업화와 임상시험을 진행하는 가운데 독일Heraeus 대웅제약 안국약품 동화약품 등과 협력하여 줄기세포치료제와 배양액의 사업화에 성공하는 등 경쟁력을 확보하고 있다. 하지만 동사의 영업적자폭이 확대되면서 외형이 축소가 진행되고 있는 상황이다. 비임상시험 부문의 견조한 수주확대와 줄기세포 화장품에 따른 신규매출 발생에도 불구하고 줄기세포배양액과 배양배지 매출 급감으로 외형은 전년(2017년) 동기대비 축소됐다. 원가가 매출액을 웃도는 가운데 판관비부담 또한 가중되면서 영업손실폭은 전년동기대비 확대됐다. 그러나 공정가치측정 금융자산 평가와 거래이익 반영으로 순손실폭은 축소됐다. 아토피 줄기세포 치료제 임상 3상진행과 줄기세포 관련 특허권의 다수 취득으로 줄기세포 부문의 매출 회복이 기대되면서 외형성장과 수익성 개선이 예상되고 있다. 동사가 속한 생물학적제제 제조업종에서 ▷삼성바이오로직스 ▷메디톡스 ▷휴젤 ▷에스케이플라즈마 ▷쎌바이오텍 등이 매출순위 기준 1~5위권에 자리잡고 있다. 강스템바이오텍은 동업종에서 21위수준으로 나타났다.
동사의 사업환경은 ▷고령화사회진입 재생의약 바이오기술의 비약적인 발전으로 시장은 더욱 활성화 될 것으로 전망되며 ▷고부가가치 창출을 통한 고수익 사업으로 성장할 예상되고 있고 ▷연구개발에 소요되는 개발기간이 길고 준수해야 하는 제약조건이 많으며 진입장벽이 높아 제품 개발에 성공한 경우 시장 내에서 독점적 지위를 누리게 되며 ▷정부에서 줄기세포 임상시험 관련 주요 규제를 철폐하면서 줄기세포분야의 성장을 지원하는 등 줄기세포치료제 강국을 지향하는 후속 정책을 추진중이다. 동사는 경기변동과 계절적 요인에 따른 민간도가 비교적 낮으며 비탄력적인 성향을 보인다.
주요제품은 ▷줄기세포배양액(7.9%) ▷줄기세포치료제(1.2%) ▷화장품사업부 (29.6%) ▷연구용역사업부 비임상시험 (60.9%) 등으로 구성된다. 경기변동이나 계절적요인과 관련 동사는 민감도가 비교적 낮고 비탄력적이다. 원재료는 실험용배지가 대부분이다. 동사의 설적변수는 해외진출시 시장이 더욱 확대될 것으로 예상되며 신약개발의 성공 여부 역시 실적에 직결된다. 동사의 재무건전성은 중간등급으로 ▷부채비율24% ▷유동비율4146% ▷자산대비차입금비중20%
▷최근4분기합산 영업익적자 등으로 나타났다. 신규사업으로 ▷동물임상시험 TRACS(Translational Research and Animal Clinical Study)에 착수했다. 이를 통해 임상시험의 성공률 향상을 목표로 삼고 있다.
국내시장 1,500억원 시장을 목표로 삼아
강스템바이오텍(217730) 제대혈 줄기세포기반 신약Pipeline 임상 중
종목리서치 | 골든브릿지투자증권 하태기 |
독자적 줄기세포 대량생산 기술 확보, 다양한 신약 Pipeline 개발 중
강스템바이오텍은 제대혈 줄기세포를 기반으로 다양한 신약 Pipeline를 개발하는 바이오기업이다.
2012년에 줄기세포GMP센터를 준공했다.
독자적인 줄기세포 분리 및 대량배양기술을 확보한 상태에서 현재 유상증자 자금으로 공장건설을 진행(2020년 생산목표)하고 있다.
향후 동종 줄기세포를 이용, 대량생산하게 됨에 따라 임상에 성공하여 제품승인을 받기만 하면 상업성 있는 제품매출은 기대할 수 있는 상황이다.
신약 Pipeline으로는 아토피 피부염치료제 Furestem AD, 류마티스 관절염치료제 Furestem RA, 건선치료제 Furestem CD, 퇴행성 골관절염치료제 Furestem OA 등이 있다.
또한 자회사로 화상피부치료제 등 치료제를 개발하는 DNK(지분 50%), 화장품원료(줄기세포 배양액)사업을 하는 라보셀(지분 63%),비임상 CRO사업을 하는 크로엔(지분 62%)이 있다.
현재 아토피치료제 임상3상 결과 관찰단계, 하반기 발표될 임상데이터 결과가 중요
동사의 기업가치는 대부분 신약 Pipeline에 있다.
첫째 아토피 피부염치료제 Furestem AD이다.
국내 임상 3상이 진행 중인데, 2018년 4월에 첫 환자 등록/투여가 시작되어 2018년 12월까지 195명에 대한 투여(단회투여)가 마무리되었고, 현재 관찰 중이다.
2019년 하반기에 3상 임상시험 결과보고서가 발표될 가능성이 높다.
만약 데이터가 좋게 나올 경우 2020년 품목승인을 거쳐 2021년 출시가 목표이다.
국내 1,500억원 시장을 타겟하고 있다.
자체적으로 유럽임상 2상에 대해 신청 준비단계에 있는데, 2019내 임상 2상a 허가를 신청한다는 목표이다.
두번째, 류마티스 관절염치료제 FurestemRA가 반복투여(4주 간격 3회 투여) 치료제로 임상 1/2a 계획서가 2018년 2월에 한국 식약처로부터 승인되었다.
33명의 환자대상으로 2019년 3월에 투약하고, 2020년 상반기에 결과보고서가 나올 가능성이 있다.
또한 장기과제이긴 하지만 퇴행성 관절염치료제 Furestem OA도 2017년 9월에 독일 Heraeus 메티컬과 계약을 맺고 공동으로 개발(비임상 중)을 진행중이다.
세번째, 건선치료제 Furestem CD가 현재 임상 1상 진행 중인데 투약 후 관찰 중이다.
2020년 하반기까지 전임상 완료계획이다.
전임상, 또는 임상 1상 중에 Heraeus 메티컬에 L/O 가능성도 열려 있다.
이와 같이 많은 과제가 진행 중인데, 2019년 하반기에 발표될 Furestem AD의 3상 결과가 우선적으로 주목을 받고 있다.
아토피 피부염 치료제 임상 결과에 따라 기업가치가 크게 달라질 전망
동사가 제대혈 줄기세포 기반 신약 Pipeline을 개발, 현재 다양한 임상이 진행 중이다.
특히 아토피 피부염치료제 Furestem-AD는 현재 3상 투약이 완료되고 관찰 중인데, 만약 2019년에 하반기에 임상 데이터(약효에서)가 긍정적으로
발표된다면 상업성에 대한 기대가 커질 것이다.
국내 줄기세포 치료제 개발에서 선두권 위치에 있어, 임상 결과에 따라 기업가치가 크게 달라질(변동성 포함) 것이다.
참고로 자회사도 시간의 경과에 따라 기업가치가 증가할 가능성이 있어 장기관점에서 주목된다
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 내달 지수 변경..."코스피-중형주·코스닥-대형주 노려라" (0) | 2019.02.28 |
|---|---|
| 강스템바이오텍 2019년도 상반기 인력 채용 (0) | 2019.02.28 |
| 거부반응 없는 '만능줄기세포' 세계 첫 개발 美샌프란시스코 UC 연구팀 보고, 줄기세포 유전자편집 '돌파구' (0) | 2019.02.25 |
| 제대혈 줄기세포 기반 신약Pipeline 임상 중 (0) | 2019.02.23 |
| 아토피 피부염 경쟁사 사노피의 Dupilumab 관련 내용 (0) | 2019.02.23 |
글
거부반응 없는 '만능줄기세포' 세계 첫 개발 美샌프란시스코 UC 연구팀 보고, 줄기세포 유전자편집 '돌파구'
설정
트랙백
댓글
http://www.dailymedi.com/detail.php?number=840252&thread=22r08
===============================================================
| ||||
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 강스템바이오텍 2019년도 상반기 인력 채용 (0) | 2019.02.28 |
|---|---|
| 강스템바이오텍 - 제대혈 줄기세포기반 신약Pipeline 임상중·목표가 미제시 (0) | 2019.02.27 |
| 제대혈 줄기세포 기반 신약Pipeline 임상 중 (0) | 2019.02.23 |
| 아토피 피부염 경쟁사 사노피의 Dupilumab 관련 내용 (0) | 2019.02.23 |
| 강스템바이오텍, '줄기세포 GMP 센터' 4월 완공…3.6만 바이알로 확대 (0) | 2019.02.22 |
글
GOLD BRIDGE 투자 증권 레포트
국내 임상 3상 결과 긍정적으로 나오면 회사 가치가 크게 달라짐.
이제 몇 개월 안남았다..
===================================================================
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 강스템바이오텍 - 제대혈 줄기세포기반 신약Pipeline 임상중·목표가 미제시 (0) | 2019.02.27 |
|---|---|
| 거부반응 없는 '만능줄기세포' 세계 첫 개발 美샌프란시스코 UC 연구팀 보고, 줄기세포 유전자편집 '돌파구' (0) | 2019.02.25 |
| 아토피 피부염 경쟁사 사노피의 Dupilumab 관련 내용 (0) | 2019.02.23 |
| 강스템바이오텍, '줄기세포 GMP 센터' 4월 완공…3.6만 바이알로 확대 (0) | 2019.02.22 |
| 강 경 선 교수 서울대학교 수의과대학 성체줄기연구센터 (0) | 2019.02.22 |
글
http://www.biospectator.com/view/news_view.php?varAtcId=2708
2022년 매출 4조 기대..
====================================================
2016년 FDA(미국 식품의약국)는 22개의 신약을 승인하면서 최근 6년만에 가장 저조한 성적을 보였다. 승인 신청을 제출한 신규 의약품은 41건으로 허가 신청 수 자체가 줄어든 것은 아니다.
현재 FDA 승인 결과를 기다리고 있는 신약 중에는 블록버스터 약물로 등극하거나 기존 시장을 상당히 위협할 것으로 예상되는 신약들이 눈에 띈다. 이벨류에이트 파마(Evaluate Pharma)는 로슈(Roche)의 다발성경화증 치료제 ‘오크레부스(Ocrevus, Ocrelizumab)’와 사노피(Sanofi)의 아토피 피부염 치료제 ‘두필루맙(Dupixent, dupilumab)’을 2017년 승인 신약 중 2022년 최대 매출을 올릴 신약으로 전망했다.
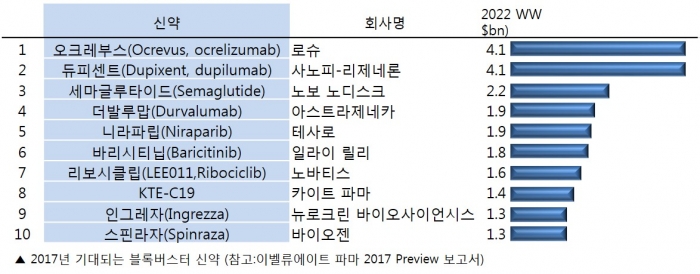
오크레부스는 신경섬유 보호막인 미엘린 수초(Myelin sheath)를 손상시켜 다발성경화증을 유발하는 B세포를 억제하는 항 CD20 단클론항체다. 대규모 임상3상시험에서 재발-완화형 다발성경화증 환자 뿐만아니라 현재 치료제가 없는 일차진행형 환자에서도 기존약물보다 뛰어난 치료 효과를 보이며 시장의 관심을 받고 있다.
사노피와 리제네론(Regeneron)이 공동 개발한 두필루맙은 중증도 이상의 아토피 환자에게 희망을 가져다 줄 신약이다. 이는 인터루킨-4 수용체(IL-4Rα) 차단을 통해 아토피 및 알레르기 질환에 관여하는 인터루킨-4(IL-4)와 인터루킨-13(IL-13)의 신호 전달을 조절하여 아토피 증상을 완화시킨다.
현재, ‘혁신 치료제(Breakthrough Therapy)’로 선정된 ‘오크레부스’와 ‘두필루맙’ 두 의약품은 오는 3월말 FDA 승인을 내다보고 있다.
우수한 임상결과와 환자의 편의성을 높여 기존 경쟁사들을 위협할 신약들도 출시될 전망이다. 당뇨질환시장의 선두주자 노보 노디스크가 개발한 1주형 차세대 GLP-1 유사체인 ‘세마글루타이드(Semaglutide)’의 등장에 일라이 릴리의 ‘트루리시티(Trulicity, Dulaglutide)’ 등 경쟁사들이 긴장하고 있다. 지난 12월, 노보 노디스크는 8000명 이상의 성인 제 2형 당뇨병 환자를 대상으로 시행한 ‘SUSTAIN 임상시험’의 우수한 결과를 기반으로 FDA 승인을 신청한 상태다.
환자의 불편을 줄인 경구용 류마티스관절염 치료제 ‘바리시티닙(Baricitinib)’의 등장도 기대된다. 이는 일라이 릴리가 개발한 것으로 화이자의 ‘젤잔즈(Xeljanz, tofacitinib)’에 이어 2번째 JAK 억제제 계열의 경구용 치료제다. 특히, 임상3상에서 전체 의약품 매출 1위로 류마티스관절염 시장을 이끌고 있는 ‘휴미라’보다 더 높은 반응률을 보이며 경구용 항류마티스제 시장을 본격적으로 열 것으로 보인다.
노바티스의 CDK 4/6 억제제 ‘리보시클립(LEE011, Rebociclib)’도 진행성 또는 전이성 유방암 1차 치료제로 FDA 승인을 기다리며 화이자가 출시한 이브란스(Ibrance)의 뒤를 바짝 추격하고 있다.
면역항암제 개발 열기는 올해도 계속 뜨겁다. 옵디보, 키트루다의 명성을 이을 아스트라제네카의 PD-L1 단클론항체 ‘더발루맙(Durvalumab)’은 요로상피암 적응증에 대해 FDA승인을 기다리며 블록버스터 면역항암제 경쟁을 가속화할 예정이다. 현재, 두발루맙은 비소세포폐암, 두경부 편평세포암종, 위암, 췌장암, 간세포암종, 혈액암 등의 적응증에 대해서도 단독 또는 병용요법으로 임상시험 연구 중이다.
2017년 빅이슈로 단연 꼽히는 CAR-T를 이용한 최초의 치료제도 처음 출시된 전망이다. 카이트 파마(Kite Pharma)의 ‘KTE-C19’는 재발성 B세포림프종 환자를 대상으로 우수한 임상시험 결과를 발표하면서 주목을 받고 있다.
블록버스터급 신약을 개발해 세간의 기대를 받고 있는 바이오 회사들도 눈에 띈다. 미국의 종양학 전문 생명공학회사 ‘테사로(Tesaro)’는 난소암 치료제로 PARP(poly(ADP)-rivose polymerase) 저해제 계열 ‘니라파립(Niraparib)’을 개발하여 지난해 11월 FDA 승인신청을 제출했다. 특히, 니라파립의 임상결과가 뛰어나다. BRCA 변이 양성 난소암 환자들을 대상으로 한 임상시험에서 니라파립 투여시 무진행 생존기간 중간값이 위약군 보다 15.5개월 가량이나 증가한 임상결과를 발표했다. 또한, BRCA 변이가 없는 환자군에서도 뛰어난 개선효과를 보이며 치료옵션이 적은 난소암 환자들에게 새로운 가능성을 열어줄 것으로 보인다. 니라파립의 가치를 반영하듯 테사로의 주가는 현재 꺾일 줄 모르고 고공행진 중이다.
샌디에고 소재의 뉴로크린(Neurocrine) 바이오사이언스도 일명 ‘틱장애’라 불리는 지연성 운동장애 치료제 ‘인그레자(Ingrezza)’ 개발해 출사표를 던졌다. FDA 승인 결과는 4월 초에 나올 예정이다.
바이오젠의 ‘스핀라자(Spinraza)’는 척수성 근육위축증에 대한 최초의 치료제로 지난해 말 FDA 승인을 받으며 등장했다. 특히, 매우 우수한 임상결과와 함께 RNA 기반 치료제로는 처음으로 블록버스터 의약품으로 성장할 가능성이 커 새로운 기대주 중 하나다.
==========================================
http://www.bosa.co.kr/news/articleView.html?idxno=2076787
2022년까지 56억 $...(6조) 매출 기대...
지난해 승인된 신약 가운데 듀픽센트(Dupixent, dupilumab)가 최대의 매출을 올릴 전망이라고 이피밴티지가 내다봤다.
이에 따르면 듀픽센트는 2022년까지 55억9000만달러의 매출이 기대되며 이어 동기간 오크레버스(Ocrevus, ocrelizumab)에 48억6000만달러, 주 1회 투여 항당뇨제 오젬픽(Ozempic, semaglutide)이 30억8000만달러, 임핀지(Imfinzi, durvalumab)가 24억8000만달러, 제줄라(Zejula, niraparib)는 16억달러로 작년 허가 신약 중 매출 다섯 손가락 안에 들 관측이다.
뒤따라 키스칼리(Kisqali, ribociclib)에 15억3000만달러, 예스카타(Yescarta, axicabtagene ciloleucel)가 13억9000만달러로 5년 뒤까지 블록버스터가 되겠고 이어 류마티스 관절염 치료제 올루미언트가 8억8000만달러, 베빅사(Bevyxxa, betrixaban)가 8억달러로 따를 예측이다.
아울러 올해 출시 기대 신약 중에선 길리어드의 빅테그라비어/F/TAF(Bictegravir/F/TAF)가 동기간 50억5000만달러의 매출로 가장 높을 것으로 꼽혔다.
이어서 면역항암제 에파카도스태트(epacadostat)가 19억4000만달러, 로바-티(Rova-T, rovalpituzumab tesirine)에 14억4000만달러, 오자니모드(ozanimod) 12억7000만달러, 아팔루타미드(apalutamide) 12억4000만달러, 엘라골릭스(elagolix) 12억1000만달러, 라나델루맙(lanadelumab)이 11억3000만달러, 에피디올렉스(epidiolex)가 10억4000만달러로 5년 뒤 블록버스터가 될 것으로 보인다.
이밖에도 올해는 척수성 근위축 유전자 치료제 AVXS-101이 신속하게 승인될 가능성도 있으며 출시되면 그 때까지 11억3500만달러의 매출이 기대된다. 또한 암 치료에 후성적으로 접근한 신약 타제메토스태트(tazemetostat)도 빠르게 소포 림프종에 허가되면 동기간 예상 매출이 8억5800만달러에 달하며 CAR-T 항암제 JCAR017 역시 올해 허가에 성공할 경우 그 때까지 8억2800만달러의 매출이 내다보인다.
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 거부반응 없는 '만능줄기세포' 세계 첫 개발 美샌프란시스코 UC 연구팀 보고, 줄기세포 유전자편집 '돌파구' (0) | 2019.02.25 |
|---|---|
| 제대혈 줄기세포 기반 신약Pipeline 임상 중 (0) | 2019.02.23 |
| 강스템바이오텍, '줄기세포 GMP 센터' 4월 완공…3.6만 바이알로 확대 (0) | 2019.02.22 |
| 강 경 선 교수 서울대학교 수의과대학 성체줄기연구센터 (0) | 2019.02.22 |
| IR ROOM 질문과 답변 (0) | 2019.02.21 |
글
http://www.etoday.co.kr/news/section/newsview.php?idxno=1724600
====================================================================
강스템바이오텍이 4월 줄기세포의 대량 생산 시스템 도입을 위한 GMP(우수의 약품 제조 및 품질관리 기준)센터 구축을 완료할 전망이다. 강스템 바이오텍은 GMP 센터에서 판매용 완제품 생산을 통한 원가 절감 및 수익성 확대를 기대하고 있다.
회사 관계자는 21일 “GMP 설비 완공예정일은 4월이며 식품의약품안전처 검증 실험 생산(Validation) 기간이 1년 정도 소요될 전망”이라며 “2020년 생산 목표는 연간 3만6000 바이알(vials, 인당 투여량)의 줄기세포 치료제 생산이 가능할 것”이라고 말했다.
GMP센터는 총면적 2600㎡ 규모로, 생산능력은 애초 계획인 연간 3만 바이알에서 3만6000 바이알로 늘렸다. 강스템바이오텍이 그동안 임상 시약 생산 시설을 보유했다면 완공 후 대량 생산 시설 확보가 이뤄지는 셈이다.
강스템바이오텍은 현재 국내 임상 3상을 진행 중인 아토피피부염 치료제 ‘퓨어스템 에이디주’를 해당 설비에서 양산할 예정이다. 류마티스 관절염 치료제. 크론병 치료제 등 차기 신약도 자체 생산한다는 구상이다.
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 제대혈 줄기세포 기반 신약Pipeline 임상 중 (0) | 2019.02.23 |
|---|---|
| 아토피 피부염 경쟁사 사노피의 Dupilumab 관련 내용 (0) | 2019.02.23 |
| 강 경 선 교수 서울대학교 수의과대학 성체줄기연구센터 (0) | 2019.02.22 |
| IR ROOM 질문과 답변 (0) | 2019.02.21 |
| 강스템바이오텍 '퓨어스템', 대웅제약의 공동개발 중단 선언… 오히려 호재? (0) | 2019.02.20 |
글
서울대학교 수의과대학 강경선 교수 연구팀은 줄기세포의 특성과 기능 및 치료효과를 연구해 왔으며, 기초, 중개 및 임상연구 단계까지 다양한 연구를 진행하고 있다. 특히, 제대혈에서 유래한 성체줄기세포의 면역조절능력 및 노화의 연구에 선도적인 역할을 해왔고, 직접분화법(Direct Conversion)을 이용하여 분화가 완료된 체세포로부터 신경줄기세포로의 직접형질전환에 대한 연구를 하고 있다. 이를 바탕으로 국내외 대학교 및 병원과 컨소시엄을 구축하여 난치성 질환의 세포치료제 개발을 위해 노력하고 있다. 나아가 인공장기를 개발하여 현 장기이식의 한계를 극복하는 대안을 제시하는 연구를 진행하고 있다.
1) 줄기세포를 이용한 면역 조절 연구
성체줄기세포, 특히 제대혈 유래 중간엽 줄기세포를 현행치료법을 통해 완치가 어려운 난치성 질환에 적용하여 그 치료효과 및 작용기전을 증명하고, 대체치료제로서의 가능성을 제시하고 있다. 이미 줄기세포의 면역조절능을 통해 크론병, 아토피 피부염, 류마티스성 관절염 등의 자가면역성 질환에 대한 효과 및 기전에 대한 연구를 발표한 바 있다. 또한 성체 줄기세포가 가지는 단점인, 개체의 차이에 기인한 세포 효능의 차이를 극복하고자 질병 특이적인 세포 효능 증진 방안에 대하여 연구를 진행하고 있다. 일례로 위 연구 결과를 통해서도 보고한 바와 같이, 줄기세포 내에NOD2 수용체가 제대혈 유래 중간엽 줄기세포 내에 존재하는 것을 발견하여, 이와 밀접한 관련을 갖는 염증성 장염에 적용하여, 그 효과가 크게 증가되는 것을 확인한 바 있다. 최근에는 위 연구 성과들을 통하여 얻어진 기술을 바탕으로 신약 혹은 나노입자 등의 치료 효능을 해당 질병에서 검증하는 부분까지 연구 범위를 확대하고 있다.

성체줄기세포를 이용해 줄기세포를 포함한 세포의 노화 및 생체 노화를 연구한다. 성체줄기세포의 노화를 유도 할 수 있는 다양한 방법을 이용해 노화 기전을 연구하고 억제 인자를 탐색한다. 이와 함께 노화 관련 질환 모델링을 통해 질환 및 일반 노화에서의 세포의 변화 기전을 밝히고 이를 통해 일반 노화를 비롯한 노화 관련 질환의 치료 및 예방 방안을 탐색한다. 히스톤 단백질 조절 인자 및 핵막 단백질 조절 인자 등을 통해 성체줄기세포의 노화 기전에 대한 보고가 있어왔다. 이러한 연구결과를 바탕으로 줄기세포 치료를 위한 최적의 세포 확보 방안을 마련하고 노화 억제를 통한 치료능의 향상도 기대할 수 있다.

생체모사체(organoid)란 "조직에서나 혹은 줄기세포에서 유래된 세포를 이용하여 이를 3D 형태로 배양을 하여 마치 인공장기와 같은 형태의 최소 기능을 할 수 있도록 만들어진 미니 유사 장기"를 의미한다. 줄기세포를 적절한 3차원 실험관 환경에서 배양하면 생체 내 기관과 유사한 구조를 형성한다는 사실이 밝혀지면서 organoid 연구를 위하여 3차원 세포배양 등이 개발되고, organoid 다양한 조직으로 분화시킬 수 있는 분화인자의 최적화 연구와 함께 주목을 받기 시작했다. 특히, 인간의 질병은 다양한 세포에 복합적으로 영향을 받는데, 이런 면에서 organoid는 좋은 질환 모델이다. 돼지 간을 이용해 인간의 장기와 구조, 기능적으로 유사하면서 면역 거부반응이 없는 '이종이식용 인공 간 제작'을 목표로 하고 있다. 이를 위해, 면역 거부 반응의 원인물질(이종항원)인 이식항원을 제거한 돼지 간 유래 탈세포 지지체(decellularized bioscaffold) 제작 및 재세포화 시 세포접합율 증가를 위한 처리방법을 개발하고 있다. 또한 직접분화법(direct conversion)을 통해 장기이식 대상 환자의 세포로부터 제작한 환자 특이적 간세포 및 혈관세포와 이번에 개발된 인공 장기 제작 기술 등을 연구, 활용하여, 최종적으로 환자 맞춤형 인공 간 개발의 상용화를 이루고자 한다. 현재까지 탈세포 지지체 유래물질을 활용하여 인간 유래 줄기세포의 간세포 분화 효율 증가 및 간 기능 증진 연구, 돼지 피부세포로부터 돼지 간 전구세포 생산 연구 등을 발표하였다. 종합적으로 돼지 간을 이용하여 탈세포화된 지지체를 제작하고 체외배양시스템과 간 및 혈관으로 분화한 줄기세포 등을 활용하여 생체모사 인공 간 제작 연구를 진행하고 있으며 향후 중동물 이식실험을 통해 인공 간의 임상 적용 가능성을 분석할 계획이다.

줄기세포를 희귀 신경질환에 치료용 목적으로 적용하기 위한 연구를 진행하고 있다. 특히 Niemann pick type C1(NPC1)이라는 희귀 질환의 치료를 목적으로 연구하고 있다. NPC1은 콜레스테롤이 세포질에 축적되면서 소뇌의 Purkinje 신경세포의 apoptosis를 일으키는, 100,000명 중 1명에게 유발하는 희귀한 신경질환이다. 치료부위가 소뇌이다 보니 줄기세포를 적용하는데 난관이 많이 존재한다. 환자에게 부담이 적은 시술경로를 이용해 최대한 효율적으로 뇌에 줄기세포를 전달하기 위한 연구를 진행하고 있다. 이외에 질환모델에서 줄기세포의 생리를 밝히는 연구도 진행하고 있다. 질환모델에서 줄기세포, 특히 신경줄기세포의 생리를 밝힘으로써 질환을 이해하고 더 나아가 치료를 위한 새로운 접근을 많이 시도하고 있다. 
루게릭 질환은 중추신경계의 운동신경세포의 사멸로 인해 수년 내에 사망에 이르는 질환으로 현재 확실한 치료제가 없어 미래사회에 있어 대단히 중요한 불치병 중에 하나이다. 본 연구는 치료제 개발을 위해 유전자치료 및 줄기세포 치료 등 여러 방법을 이용하여 루게릭 모델 동물에서의 유효성을 검증하여 치료효과 및 증상완화를 목표로 하고 있다. 
- 소속: 서울대학교 수의과대학 교수
- E-mail : kangpub@snu.ac.kr
- Tel : 02-880-1298
- 홈페이지: http://adultstemcell.snu.ac.kr
- 박사후 연구원: 최순원
- 박사과정 학생: 강인성, 김재준, 이병철, 이진영, 국명근
- 석사과정 학생: 김민수, 김다현, 강현경, 김보은, 이승은, 신나리, 배태현, 정의정
- 1. Clinical Trial of Human Umbilical Cord Blood-derived Stem Cells for the Treatment of Moderate-to-Severe Atopic Dermatitis: Phase I/IIa Studies, STEM CELLS, 2017
- 2. Cathepsin S contributes to microglia-mediated olfactory dysfunction through the regulation of Cx3cl1-Cx3cr1 axis in a Niemann-Pick disease type C1 model, GLIA, 2016
- 3. Human umbilical cord blood mesenchymal stem cell-derived PGE2 and TGF-β1 alleviate atopic dermatitis by reducing mast cell degranulation, STEM CELLS, 2015
- 4. Rapid and Efficient Direct Conversion of Human Adult Somatic Cells into Neural Stem Cells by HMGA2/let-7b, Cell Reports, 2015
- 5. Human umbilical cord blood mesenchymal stem cells reduce colitis in mice by activating NOD2 signaling to COX2, GASTROENTEROLOGY, 2013
◎ 지적재산권
- 1. 서울대학교, Equine Amniotic Fluid-Derived Multipotent Stem Cells and a Method for Producing the Same, 국제 특허 등록(미국, 등록번호 US9290739 B2, 등록일자 2015.11.06.)
- 2. 서울대학교, CD49F promoting proliferation, multipotency and reprogramming of adult stem cells through PI3K/AKT/GSK3 pathway, 국제 특허 등록(미국, 등록번호US9139812 B2, 등록일자2015.09.22.)
- 3. 서울대학교, Pharmaceutical composition comprising stem cells treated with NOD2 agonist or culture thereof for prevention and treatment of immune disease and inflammatory diseases, 국제 특허 등록(일본, 등록번호5805195, 등록일자2015.09.11.)
- 4. 서울대학교, Isolating method for umbilical cord blood-derived pluripotent stem cells expressing ZNF281, 국제 특허 등록(호주, 등록번호CN102395673 B, 등록일자2014.06.26.)
- 5. 서울대학교, Multipotent adult stem cells having an ability of oct4 expression derived from umbilical cord blood and method for preparing the same, 국제 특허 등록(유럽, 등록번호EP1954803 B1, 등록일자2013.05.22.)
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 아토피 피부염 경쟁사 사노피의 Dupilumab 관련 내용 (0) | 2019.02.23 |
|---|---|
| 강스템바이오텍, '줄기세포 GMP 센터' 4월 완공…3.6만 바이알로 확대 (0) | 2019.02.22 |
| IR ROOM 질문과 답변 (0) | 2019.02.21 |
| 강스템바이오텍 '퓨어스템', 대웅제약의 공동개발 중단 선언… 오히려 호재? (0) | 2019.02.20 |
| 기타 경영사항(특허권 취득)(자율공시) (0) | 2019.02.19 |
글
https://m.irgo.co.kr/ir-room/3202/%EA%B0%95%EC%8A%A4%ED%85%9C%EB%B0%94%EC%9D%B4%EC%98%A4%ED%85%8D-IR-ROOM
FURESTEM AD (아토피 치료제) 는 국내 임상 3상 완료 후 몇 개월 후 결과 발표될 예정임.
임상 결과 발표 전/후 국내 판매 대행을 위해 국내 제약사와 판권 계약 진행
해외 판권은 해외 빅파마에게 L/O 형태로 진행할 계획
임상 3상 결과는 기존 임상 자료와 3개년 장기 추적 결과 등을 통해 어느정도 예측 가능함.
국내 제약사와 판권 계약 그리고 해외 임상 진행 ..무엇보다 L/O 체결되면 이 회사 주식은 5년 이상은 보유해야함.
======================================================================
이번에 대웅제약과 계약변경으로 새로운 업체과 계약을 진행하는 걸로 알고 있습니다.
언론에서는 국내업체라고 하던데, 국내판권, 해외판권 모두 국내업체에서 하는건가요?
아님 국내판권만 국내업체에 해외판권은 해외 제약사와 계약하는 건가요?
IR담당자2019.02.20 13:28
네....국내업체입니다.
아시다시피, 국내는 이미 임상 3상까지 진행한 상황이라 라이센싱 아웃이 아닌 판권(판매대행) 계약으로 진행하고 있습니다. 아직 해외는 임상 2상도 진행하지 않은 상황이므로, 판권은 국내판권에만 국한됩니다.
해외 판권은 해외 기업에게 라이센싱 아웃하는 형태로 진행하고자 합니다.
안녕하세요. 다름이아니라 대웅제약과 계약변경으로 인한 패널티는 없는지가 궁금합니다.
IR담당자2019.02.20 13:52
네...답변드리겠습니다.
일단 계약변경에 따른 패널티는 없습니다.
우선, 에이디주 관련 3상 비용은 저희 회사가 부담하고 있어서 계약 변경에 따라 정산할 부분은 없습니다.
그리고, 계약의 해지가 아닌 부분 변경이므로 계약금 반환과 같은 이슈도 없습니다.
아울러, 말씀드릴 부분은 대웅제약은 여전히 저희의 중요 파트너입니다. 비록 아토피에서는 협력관계가 없을수 있으나, 류머티스 등의 주요 파이프 라인에서는 여전히 파트너 관계가 유효합니다.
감사합니다.
이번 AD는 강스템에서 독자적으로 개발및 임상을 하여 대웅과 해지 하였다고 하면
CD와 RA는 대웅과 협업하여 개발한것인지 문의 드립니다.
또한 Ra와 CD역시 강스템에서 독자 개발및 임상을 진행한것이라고 하면
차후 대웅과 해지 할 계획이 있는지요??
그리고 주가 안오른다고 징징거리는 질문같지도 않은 질문까지도 답변해주셔서 믿음이 갑니다.
IR담당자2019.02.20 14:07
우선, 계약의 해지는 아닙니다.
해당 계약은 저희가 상장하기 전에 체결된 포괄 계약이었습니다.
즉, 개별 파이프라인별로 가치를 일일히 산정해서 진행했던 계약은 아닌 걸로 알고 있습니다.
따라서, 시간이 지나면서 파이프라인별로 확정되지 않았던 부분들이 구체화되는 과정에서 생각은 충분히 다를수 있다고 생각합니다.
그리고, 대웅제약은 여전히 저희의 중요 파트너사입니다.
다만, 에이디주 관련해 협력관계가 없을 수 있으나, 자가면역질환 관련 파이프라인에서는 기존의 협력관계가 유효합니다.
따라서, 류머티스 등의 파이프라인들과 향후 개발하게 되는 자가면역질환 치료제는 대웅과 협업하게 될 계획입니다.
감사합니다.
AD 임상이 끝나고 시판이 가까워 지는 시점에서 대웅이 AD를 포기한 이유가 무척 궁금합니다.
2. 향후 국내판권을 갖게 될 회사는 확정되었는지요?
3. 기술수출건은 현재 어느 정도 진행되고 있는지 궁금하네요.
4. CD(크론) 임상2상에 대한 계획은 정해졌나요?
IR담당자2019.02.20 14:19
네...답변 드리겠습니다...
1. AD 임상이 끝나고 시판이 가까워 지는 시점에서 대웅이 AD를 포기한 이유가 무척 궁금합니다.
=> 사실, 양사간 세세한 내용을 공개적으로 밝히는 것은 부담스러운 일입니다. 그리고 계약이 파기된 것이 아니고, 변경이 된 것이기 때문에 여전히 양사는 계약관계에 있는 파트너사라는 점도 언급이 조심스럽습니다.
다만, 에이디주에 대한 생각이 다소 달랐던 점은 사실이고, 저희 요청에 따라 검토를 시작했고, 양사가 원만하게 합의를 통해 계약이 변경된 사항이라는 점은 말씀드릴수 있을거 같습니다.
아울러, 일부에서 언급되는 에이디주의 효능상 문제 있어서 변경한 것이 아니냐는 우려는 사실이 아닙니다.
에이디주는 현재 임상 3상이 진행중이며, 이중맹검이 되어 있어 사실 저희 회사도 의사도 효능에 대한 구체적인 결과를 알지 못합니다. 이런 상황에서 에이디주의 효능을 먼저 알았다는 점은 억측에 가깝다고 생각합니다.
2. 향후 국내판권을 갖게 될 회사는 확정되었는지요?
=> 네...현재 진행중에 있습니다. 빠른 시일내에 아토피 판권 계약을 마무리할 수 있도록 하겠습니다. 그리고 적시성 있게 알려드릴수 있도록 하겠습니다.
3. 기술수출건은 현재 어느 정도 진행되고 있는지 궁금하네요.
=> 해외 라이센스 아웃 협상은 진행중인 기업은 있다고 전해들었습니다.
다만, 구체적으로 밝히기는 어려운 점은 양해부탁드립니다. 공개적으로 대외에 구체적인 협상 내용을 누설하는 행위가 협상에 부정적인 영향을 미치기 때문입니다.
향후에 가시적인 성과가 나오면 바로 알려드릴수 있도록 하겠습니다.
4. CD(크론) 임상2상에 대한 계획은 정해졌나요?
=> 사실 고민이 많은 부분입니다. 일단 크론병 관련 임상 1상이 국내에서는 쉽지 않았던 점은 알고 계실거 같습니다. 따라서, 지금은 계속 국내 임상 2상으로 진행할지, 해외임상으로 진행할지, 아니면 다른 대안을 찾을지 내부적으로 고민 중에 있습니다.
만일 결정되면, 적절한 방법으로 적시성 있게 알려드리도록 하겠습니다
'바이오종목 > 강스템바이오텍' 카테고리의 다른 글
| 강스템바이오텍, '줄기세포 GMP 센터' 4월 완공…3.6만 바이알로 확대 (0) | 2019.02.22 |
|---|---|
| 강 경 선 교수 서울대학교 수의과대학 성체줄기연구센터 (0) | 2019.02.22 |
| 강스템바이오텍 '퓨어스템', 대웅제약의 공동개발 중단 선언… 오히려 호재? (0) | 2019.02.20 |
| 기타 경영사항(특허권 취득)(자율공시) (0) | 2019.02.19 |
| "정밀의료·줄기세포·유전자치료 통과? 규제 강화할 대상" (0) | 2019.02.19 |





RECENT COMMENT