검색결과 리스트
바이오종목/제넥신에 해당되는 글 68건
- 2018.10.30 네오이뮨텍, 하이루킨-7+표준 "美FDA 뇌암 1b/2a상 승인"
- 2018.10.16 제넥신, 단장증후군 치료제 'GLP-2' 美 FDA 희귀의약품 지정
- 2018.10.10 [마켓인]네오이뮨텍, 프리IPO로 1500억 투자유치 나선다
- 2018.10.10 [기고]2018년 노벨 생리의학상 수상의 시사점
- 2018.10.05 넥타 '인터루킨 면역항암제' 실패설…불안심리 확산
- 2018.10.01 "제넥신, 11월 면역항암제 학회 후 R&D 모멘텀 주목"
- 2018.09.29 "글로벌 전문가 모셔라"…바이오 업체 잇단 영입
- 2018.09.28 제넥신 "지속형 성장호르몬 2상, 12개월서도 효과 확인"
- 2018.09.23 면역항암제 병용투여 강력후보 제넥신 하이루킨 기대↑
- 2018.09.21 제넥신, CPA 전처리 후 면역항암제 투여 1b상 진입
글
http://biospectator.com/view/news_view.php?varAtcId=6458
바이오스펙테이터 김성민 기자
총 46명 뇌암(HGG) 대상 약물 안전성 및 효능 평가..."HGG 면역세포 고갈된 상태, 하이루킨-7 투여로 T세포 증가...임상적 유효성 기대"

▲양세환 네오이뮨텍 대표
네오이뮨텍은 미국 식품의약국(FDA)으로부터 새롭게 진단받은 뇌암(high grade glioma, HGG) 환자에게 표준치료와 하이루킨-7(hyleukin-7, NT-I7)을 병용투여하는 임상1b/2a상을 승인받았다고 29일(미국 현지기준) 밝혔다. 하이루킨-7은 T세포 숫자를 늘리고, 기능을 높이는 면역항암제다.
이번 임상은 총 46명 환자를 대상으로 약물 안전성 및 효능을 확인하며, 워싱턴대 의과대학의 지안 캠피안(Jian Campian) 박사 연구팀과 공동으로 진행한다. 임상에서 용량을 찾으면, 바로 상업화를 위한 임상 2상으로 돌입하는 프로토콜로 진행한다.
NgocDiep Le 네오이뮨텍 최고 의학책임자(CMO)는 "이번 임상은 혁신적인 면역 약물인 하이루킨-7이 화학치료 및 방사선치료를 받은 뇌암 환자에게서 림프구 숫자를 늘리고, 병기진행에 주는 영향을 평가하기 위해 진행한다"며 "기존 치료만으로는 나쁜 예후를 보인 HGG 환자에게 하이루킨-7은 T세포 숫자를 늘리고 임상적 유효성을 줄 것으로 예상한다"고 설명했다.
대부분 HGG 환자는 면역세포가 고갈된 상태로, 해당 환자에게서 이러한 현상은 생존률을 낮춘다고 보고돼 있다. 현재 네오이뮨텍은 제넥신과 표준치료를 받은 뇌암 환자에게 하이루킨-7을 투여해 약물 안전성 및 내약성을 확인하는 국내 임상/1상을 진행하고 있다. 또한 네오이뮨텍은 미국 암연구소(NCI)의 지원을 받아 방사선 치료를 받은 악성 뇌교종(malignant glioma) 환자 가운데 심각한 림프구 감소증을 보이는 환자를 대상으로 임상 1상을 진행하고 있다.
한편 네오이뮨텍은 이날 항암제 후기 임상부터 최종 제품 승인까지 다년간의 신약개발 경험을 가진 NgocDiep Le 박사를 최고의학책임자(CMO)로 영입했다고 밝혔다. Le 박사는 칼텍을 거쳐 스탠포드 대학에서 의학박사 학위를 받고, 암젠, GSK, 노바티스, 메드이뮨 등 여러 빅파마 및 바이오텍에서 항암제개발을 이끌었다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| 제넥신-I-Mab, 中서 하이루킨-7 고형암 1상 승인 (0) | 2018.11.02 |
|---|---|
| 네오이뮨텍, 'NT-I7' 4가지 차별성 근거한 IO 개발전략 (0) | 2018.11.01 |
| 제넥신, 단장증후군 치료제 'GLP-2' 美 FDA 희귀의약품 지정 (0) | 2018.10.16 |
| [마켓인]네오이뮨텍, 프리IPO로 1500억 투자유치 나선다 (0) | 2018.10.10 |
| [기고]2018년 노벨 생리의학상 수상의 시사점 (0) | 2018.10.10 |
글
http://www.newspim.com/news/view/20181015000697
[서울=뉴스핌] 김양섭 기자 = 제넥신은 개발중인 단장증후군(SBS:Short Bowel Syndrome) 치료제 GLP-2(GX-G8)에 대해 미국 FDA로부터 최근 희귀의약품 지정을 받았다고 15일 밝혔다.
제넥신 관계자는 "GLP-2는 미국시간으로 지난 11일 희귀의약품에 지정됐다"면서 제넥신 "희귀질환인 SBS (Short Bowel Syndrome) 관련해 이미 시판된 가텍스(Gattex) 대비 좋은 비임상 결과를 바탕으로 CRO(임상시험수탁기관) 측과 논의해 문서를 작성했으며 그 효력 결과를 근거로 FDA ODD grant(희귀의약품 지정)을 받았다"고 설명했다.
희귀의약품으로 지정되면 정부기관의 임상 리뷰등에서 발생하는 수수료가 적게 들고 개발기간을 단축시킬 수 있는 장점이 있다. 또 임상 2상 단계에서 조건부 판매가 가능하다.
제넥신 관계자는 GLP-2 (GX-G8)의 개발단계에 대해 "현재 전임상이 완료된 상태이며 임상 1상을 준비중"이라고 설명했다.
단장증후군은 선천성 또는 생후 수술적 절제로 전체 소장 50% 이상이 소실돼 흡수장애와 영양실조를 일으키는 질환이다. 소장 점막 표면적의 감소와 담즙산의 부족, 소장 내병균 이상 증식 등 기능 이상이 동반돼 증상을 일으키는데, 소장의 절제 범위와 남아있는 부위에 따라 흡수 장애의 정도, 그리고 정맥영양에의 의존도가 달라진다. 대부분의 환자들은 일정기간 인위적인 영양보충이 필요하다. 심한 경우 생명을 위협하기도 하며, 30%정도의 사망률을 보이는 것으로 알려져 있다.세계 단장증후군 발생률은 인구 10만명 당 24.5명 꼴이다. 국내 환자 수는 1만2000여명으로 추산된다.
현재는 희귀질환전문 제약사 샤이어가 개발한 가텍스가 유일한 치료제다. 국내에서도 지난 8월 처음으로 '가텍스'가 판매 허가를 받았다.
 |
| [이미지=제넥신] |
'바이오종목 > 제넥신' 카테고리의 다른 글
| 네오이뮨텍, 'NT-I7' 4가지 차별성 근거한 IO 개발전략 (0) | 2018.11.01 |
|---|---|
| 네오이뮨텍, 하이루킨-7+표준 "美FDA 뇌암 1b/2a상 승인" (0) | 2018.10.30 |
| [마켓인]네오이뮨텍, 프리IPO로 1500억 투자유치 나선다 (0) | 2018.10.10 |
| [기고]2018년 노벨 생리의학상 수상의 시사점 (0) | 2018.10.10 |
| 넥타 '인터루킨 면역항암제' 실패설…불안심리 확산 (0) | 2018.10.05 |
글
10일 벤처캐피털(VC) 업계에 따르면 네오이뮨텍은 1000억~1500억원 규모의 투자유치를 준비 중이다. 보통주 발행 등 다양한 조달 방법이 논의되고 있지만 아직 조달방법이 확정되지는 않았다. 네오이뮨텍 측은 회사 및 제넥신에 투자했던 기존 투자가들에게 투자 우선권을 준 뒤 신규 투자가들을 유치해 자금 조달을 할 계획이다. 이번 프리IPO는 올해 안에 마무리할 전망이다.
네오이뮨텍은 제넥신에서 근무하던 양세환 박사가 지난 2014년 미국에서 설립한 바이오 전문 스타트업이다. 독립 이후에도 제넥신과의 관계는 계속되고 있다. 제넥신은 현재 네오이뮨텍의 지분(20.62%)을 보유하고 있고, 연구 등에서도 협업을 계속하고 있다.
네오이뮨텍은 이번 프리IPO로 확보한 자금을 제넥신과 공동 개발 중인 면역항암제 ‘하이루킨’의 연구·개발에 투입할 예정이다. 하이루킨은 면역세포인 T세포를 증폭시키고 T암세포의 발견과 파괴를 유도하는 물질로, 올해 초 미국 식품의약국(FDA)으로부터 암 환자 대상 임상 승인을 받은 바 있다.
이 면역항암제의 가능성은 이미 시장에서 한번 검증 받은 바 있다. 공동 개발사인 제넥신이 올해 3월 하이루킨 연구 개발 자금 등을 모으기 위해 투자를 유치한 결과 대규모 자금을 수혈받았기 때문이다. 당시 제넥신은 제3자 배정 유상증자와 전환사채(CB) 발행을 통해 바이오 전문 VC 인터베스트와 유한양행 등 10곳의 기관으로부터 2500억원의 자금을 조달한 바 있다. 증시에서도 이에 대한 기대감이 반영돼 제넥신의 주가는 지난해보다 두 배 가량 상승했다.
선례를 고려할 때 업계에서는 네오이뮨텍이 무난하게 투자가를 끌어 모을 것이라고 보고 있다. 네오이뮨텍이 제넥신과 공동으로 기술 개발에 나설 만큼 깊은 관계를 유지하고 있기 때문에 시장에서 충분히 가치를 인정받을 수 있다는 분석이다.
한 IB업계 관계자는 “제넥신과 네오이뮨텍이 개발하고 있는 면역항암제가 성공할 가능성이 크다는 시장의 평가를 받고 있다”며 “특히 제약 부문은 미국 및 유럽 등 선진 시장 규모 워낙 크기 때문에 미국을 사업 기반으로 둔 네오이뮨텍에 대한 관심도 클 것”이라고 전망했다.
다만 이번 프리IPO에는 기존 투자가보다는 신규 투자가의 참여가 두드러질 전망이다. 제넥신이 투자 유치에 성공하며 기업 가치를 인정받은 만큼 네오이뮨텍이 발행할 신주나 전환사채(CB)의 가격도 높아질 가능성은 충분하다. 기존 투자가로서는 굳이 높은 가격에 포트폴리오가 중복되는 투자를 할 유인이 크지 않다는 것이다.
제넥신에 투자를 진행했던 한 업계 관계자는 “기존 투자가 중 높은 밸류에이션에 네오이뮨텍에 자금을 댈 곳은 많지 않을 것”이라며 “다만 네오이뮨텍의 성장 가능성이 높은 만큼 많은 신규 투자가들이 관심을 갖고 투자를 문의 중이다”고 설명했다.
한편 네오이뮨텍은 지난 4월 하나금융투자를 상장주관사로 선정하고 코스닥 시장 상장을 본격화했다. 네오이뮨텍과 하나금투는 내년 하반기 상장을 목표로 ‘테슬라 요건 상장’ 등 다양한 상장 방법을 고려하고 있다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| 네오이뮨텍, 하이루킨-7+표준 "美FDA 뇌암 1b/2a상 승인" (0) | 2018.10.30 |
|---|---|
| 제넥신, 단장증후군 치료제 'GLP-2' 美 FDA 희귀의약품 지정 (0) | 2018.10.16 |
| [기고]2018년 노벨 생리의학상 수상의 시사점 (0) | 2018.10.10 |
| 넥타 '인터루킨 면역항암제' 실패설…불안심리 확산 (0) | 2018.10.05 |
| "제넥신, 11월 면역항암제 학회 후 R&D 모멘텀 주목" (0) | 2018.10.01 |
글
http://biospectator.com/view/news_view.php?varAtcId=6324
==================================================
항암제 패러다임 바꾼 CTLA-4 PD-1 면역항암제, 기초 연구에서 시작해 우여곡절 겪은 후 탄생...수많은 연구자들의 신념∙소신의 결과물

2018년 노벨생리∙의학상을 면역관문억제제(immune checkpoint blockade) 개발에 대한 공로로 제임스 앨리슨 박사(미국 택사스대학 MD Anderson 암센터)와 타스쿠 혼조 박사(교토대)가 공동 수상한다는 발표가 났을 때 관련 분야 대부분의 사람들이 ‘놀랍지 않다’는 반응을 보였다. 2010년 이후 암치료의 대세로 자리잡고 있는 항암면역치료가 노벨상 주제가 될 것이라는 것과, 이 두 분이 노벨상을 수상할 것이라는 것은 모두가 예측하고 있을 정도로 자명한 일이었다. 언제 받을 것인가와 노벨상은 3명까지 받을 수 있으니 이 두 분을 제외하고 제3의 수상자가 누가 될 것인가 정도의 의문이 있었는데, 그것이 '올해'가 되고, '제3의 공동 수상자는 없다’는 정도가 약간의 놀라움이었다.
표준 항암 치료법으로 사용되어온 수술, 방사선요법, 화학요법의 경우 암세포를 직접적으로 제거하여 암을 치료한다는 점에서 공통점을 가진다. 반면, 항암면역치료법은 생체의 면역기능의 강화를 통해 간접적으로 암을 치료한다는 점에서 개념적으로 다른 치료법이다. 이러한 개념적 차이점(혹은 지나치게 혁신적인 개념) 때문에, 항암면역치료법은 최근까지 주류 종양학자들에게 외면당해왔다. 항암면역치료법이 본격적으로 주목받기 시작한 것은, 2010년 이후 면역관문억제제와 또 다른 항암면역치료법인 CAR-T(chimeric antigen receptor T) 세포치료법이 임상에서 놀라운 치료 효능을 입증하면서부터이며, 현재는 새로운 표준치료법으로서 자리잡아가고 있다.
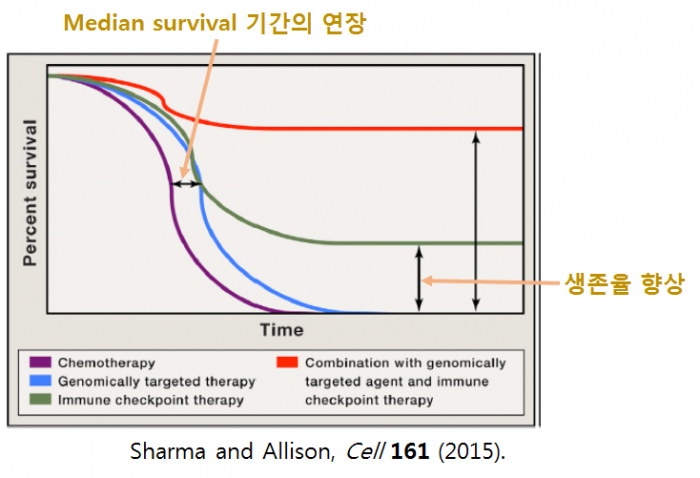
생체의 면역기능의 강화를 통하여 암을 치료하는 면역항암제가 기존 항암제와 치료 효능 측면에서 가지는 본질적인 차이는 앨리슨 박사가 2015년 Cell지에 발표한 논문의 그림을 보면 쉽게 이해할 수 있다. 기존 항암제가 난치성 종양환자의 중간 생존기간 (median survival)을 어느 정도 연장시켜주는 효능을 가졌다면(파란색 선), 면역항암제는(일부 환자이긴 하지만) 장기 생존(혹은 완치)을 가능하게 해 주는 치료법(녹색 선)이라는 측면에서 본질적인 차이를 가진다. 이러한 차이점은 기존 항암제가 암세포를 단순히 죽이는데 반해, 면역항암제는 면역 세포의 활성화 및 면역 기억 형성을 통하여 보다 능동적으로 암세포에 대응하는 본질적인 기전의 차이에서 기인한다.
중요한 점은, 이러한 면역항암제가 원래 ‘항암제’를 목표로 개발된 것이 아니라 ‘기초연구’ 과정의 부산물로서 개발되었다는 것이다. 1990년을 전후로 면역 활성에 관여되는 많은 분자들이 발견되고 그 기능을 규명하는 연구가 활발하게 이루어지기 시작하였다. 가장 먼저 밝혀진 것이 면역기능의 가속 페달에 해당하는 기능을 가지는 CD28이고, 이후 발견된 CTLA-4는 CD28와 비슷한 구조와 동일한 리간드를 가지는 측면에서 처음에는 또 다른 가속 페달의 기능을 가질 것이라고 사람들이 추정하고 있었다. CTLA-4의 기능을 차단하는 항체인 anti-CTLA-4를 개발한 이유는, CTLA-4의 기능을 규명하기 위함이었으며, 이를 통하여 CTLA-4가 면역기능을 향상시키는 가속 페달이 아닌 면역 기능을 저해하는 브레이크 기능을 가지는 것을 밝히게 된다.
흥미로운 것은, anti-CTLA-4를 이용한 CTLA-4의 기능을 규명하는 연구를 앨리슨 박사가 최초로 한 것이 아니라는 것이다. 1994년 CTLA-4의 ‘negative immune regulator’로서의 기능을 최초로 당시 신생 저널인 Immunity에 발표한 제프 블루스톤 박사는 이후 CTLA-4의 면역억제 기능에 주로 초점을 맞춰 다양한 자가면역질환 치료에 전념한다. 반면 1년 뒤인 1995년 Journal of Experimental Medicine(JEM)에 또 다른 anti-CTLA-4 항체를 이용하여 비슷한 내용을 발표한 앨리슨 박사는 ‘발상의 전환’을 통하여 anti-CTLA-4가 면역기능의 억제를 풀어 면역기능을 활성화시켜 암을 치료할 수 있는 ‘새로운 개념의 항암제’로서 활용 가능하지 않을까라고 생각하게 되고, 이러한 발상의 전환이 노벨상 수상의 근간이 되었다. 이러한 개념은 생쥐 모델에서 anti-CTLA-4의 항암 효능을 검증한 결과를 1996년 Science에 발표하면서 학문적으로 인정받게 된다.
그러나, ‘면역기능 향상을 통하여 암을 치료한다’는 개념은 당시 지나치게 혁신적인 것이라 주류 제약업계에서 받아들이지 않아 큰 어려움을 겪게 된다. 우여곡절 끝에 결국 Medarex라는 회사를 통하여 임상에 사용할 수 있는 항체를 만들고, 2003년 PNAS에 임상 1상 결과를 발표하게 된다. 이후 Medarex를 인수한 BMS가 2010년 New England Journal of Medicine(NEJM)에 anti-CTLA-4의 임상 3상 성공 논문을 게재하고, 2011년 미국 FDA 승인을 받으면서 본격적인 항암면역치료제 시대가 열리게 된다.
앨리슨 박사가 CTLA-4의 기능 연구에서 발상의 전환을 통하여 면역관문억제제 개념을 제시하고 증명하였다면, 혼조 박사는 새로운 면역관문분자인 PD-1을 최초로 발견하고(1992년 EMBO Journal), PD-1이 결핍한 쥐를 만들어서 그 기능을 규명(1999년 Immunity)하는 등 PD-1 관련 기초 연구의 상당부분을 주도하였다. 재미있는 일화는 PD-1 결핍 쥐를 만들었는데, 쥐가 태어난 후 3개월 동안 너무 건강하여 관련 연구를 수행한 학생이 스트레스를 받았다는 것이다. 수개월의 기다림 후에 PD-1 결핍 쥐에서 자가면역질환이 발견되어 PD-1의 ‘negative immune regulator’로서의 기능이 증명되는데, 이것은 CTLA-4 결핍 쥐가 수 주 이내에 심각한 자가면역질환으로 죽는 것과 대비되는 결과로, anti-PD-1이 anti-CTLA-4에 비해 훨씬 더 부작용이 적을 수 있다는 것을 암시한다. 이러한 결과에 기반하여, 혼조 박사는 anti-PD-1이 anti-CTLA-4와 같은 면역관문억제 기반의 항암제로 작용할 수 있을 뿐만 아니라 부작용이 더 적어, 보다 보편적으로 활용 가능할 것이라는 가능성을 보게 되고, 관련 연구를 본격적으로 착수하게 된다.
학문간의 경계에 대해 보수적이고 제약관련 산업이 상대적으로 약한 일본에서 기초 면역학을 전공한 혼조 박사가 anti-PD-1을 신개념의 항암제로 추진하기 위해 걸어야 했던 길은 험난했다. 우선 교토대학에서 관련 경험이 없어 ‘산업체 파트너 없이 특허를 지원해줄 수 없다’고 하여 예전에 다른 일로 협력했던 Ono Pharmaceutical을 통하여 특허를 출원할 수 밖에 없었으며, Ono의 역량 또한 임상을 위한 항체 개발 및 임상시험을 하기에는 부족했기에 결국 미국의 Medarex를 통하여 임상용 항체를 제조할 수 밖에 없었다.
2009년 Medarex를 인수한 BMS는 항암면역치료의 강자로 부상하게 되고, 이는 일본 입장에서는 자국에서 개발한 신개념 블록버스터 신약이 다국적 제약회사로 넘어가게 된 뼈아픈 경험이 아니었을까 생각된다. Anti-PD-1은 2012년 이후 다수의 NEJM 논문을 통하여 임상 약효의 수월성을 입증하고, 2014년에 FDA 승인을 받게 되고 (BMS와 Merck), anti-CTLA-4에 비해 더 부작용이 적고 효능이 좋아, 현재 가장 보편적으로 사용되고 있는 항암면역치료제로 자리잡게 되었다.
이렇게 기초연구가 발상의 전환을 통해 많은 암환자를 치료한 신개념의 항암제가 되었으며, 그 공적을 인정받아 앨리슨 박사와 혼조 박사가 2018년 노벨 생리의학상을 공동 수상하게 된 것이다. 이 두 분의 공적이 워낙 탁월하여 이 분들의 노벨상 수상에 있어서 대부분 큰 이견이 없을 것이라 생각하지만, 이러한 성공의 이면에서 노력한 수 많은 unsung heroes들의 공적 또한 무시할 수 없을 것이다.
‘항암면역치료’라는 개념 자체가 받아들여지지 않던 어려운 시절의 정신적 지주 역할을 한 Lloyd Old 박사(현대 항암면역치료의 아버지라 불리우며, 2011년 전립선 암으로 돌아가지 않으셨다면 공동 수상했을 가능성이 컸다고 개인적으로 생각)를 포함한 관련 연구를 소신있게 수행한 연구자들 (Lieping Chen, Robert Schreiber, Steven Rosenberg 등), 많은 제약회사들이 외면할 때 항암면역치료제 개발 및 임상시험을 추진한 Medarex와 BMS의 과학자 및 경영진들(Francis Cuss, Axel Hoos 등), 새로운 개념의 항암치료제의 임상 적용에 앞장서 결국 임상시험을 성공시킨 의사들(Stephen Hodi, Jedd Wolchok 등) 및 관련 연구를 묵묵히 수행한 수 많은 학생/연구원들(필자의 포닥 지도교수인 Max Krummel 등)의 노력 등이 모두 합쳐져서 오늘의 영광이 가능하게 된 것이다.
앨리슨 박사와 혼조 박사는 기초과학에서 시작하였다는 점과, 자신의 연구 결과가 항암치료에 활용 가능할 것이라는 신념을 가지게 된 이후로 주변의 회의적인 시선에 굴하지 않고 소신있게 끝까지 추진하였다는 점에서 공통점을 가지며, 이러한 점이 후학들에게 많은 시사점을 준다고 생각한다.
참고문헌
1. Ishida, Y., Agata, Y., Shibahara, K., & Honjo, T. (1992). Induced expression of PD-1, a novel member of the immunoglobulin gene superfamily, upon programmed cell death. EMBO J., 11, 3887.
2. Krummel, M. F., & Allison, J. P. (1995). CD28 and CTLA-4 have opposing effects on the response of T cells to stimulation. J. Exp. Med., 182, 459.
3. Leach, D. R., Krummel, M. F., & Allison, J. P. (1996). Enhancement of antitumor immunity by CTLA-4 blockade. Science, 271, 1734.
4. Nishimura, H., Nose, M., Hiai, H., Minato, N., & Honjo, T. (1999). Development of Lupus-like Autoimmune Diseases by Disruption of the PD-1 gene encoding an ITIM motif-carrying immunoreceptor. Immunity, 11, 141.
5. Hodi, F.S., Mihm, M.C., Soiffer, R.J., Haluska, F.G., Butler, M., Seiden, M.V., Davis, T., Henry-Spires, R., MacRae, S., Willman, A., Padera, R., Jaklitsch, M.T., Shankar, S., Chen, T.C., Korman, A., Allison, J.P. & Dranoff, G. (2003). Biologic activity of cytotoxic T lymphocyte-associated antigen 4 antibody blockade in previously vaccinated metastatic melanoma and ovarian carcinoma patients. Proc Natl Acad Sci USA, 100, 4712.
6. Hodi, F.S., O’Day, S.J., McDermott, D.F., Weber, R.W., Sosman, J.A., Haanen, J.B., Gonzalez, R., Robert, C., Schadendorf, D., Hassel, J.C., Akerlet, W., vea den Wertwegh, A.J.M., Lutzky, J., Lorigan, P., Vaubel, J.M., Linette, G.P., Hogg, D., Ottensmeier, C.H., Lebbe, C., Peschel, C., Quirt, I., Clark, J.I., Wolchok, J.D., Weber, J.S., Tian, J., Yellin, M.J., Nichol, G.M., Hoow, A., and Urba, W.J., (2010). Improved Survival with Ipilimumab in patients with metastatic melanoma. N Engl. J. Med. 363, 711.
'바이오종목 > 제넥신' 카테고리의 다른 글
| 제넥신, 단장증후군 치료제 'GLP-2' 美 FDA 희귀의약품 지정 (0) | 2018.10.16 |
|---|---|
| [마켓인]네오이뮨텍, 프리IPO로 1500억 투자유치 나선다 (0) | 2018.10.10 |
| 넥타 '인터루킨 면역항암제' 실패설…불안심리 확산 (0) | 2018.10.05 |
| "제넥신, 11월 면역항암제 학회 후 R&D 모멘텀 주목" (0) | 2018.10.01 |
| "글로벌 전문가 모셔라"…바이오 업체 잇단 영입 (0) | 2018.09.29 |
글
인터루킨-2(IL-2)를 활용한 차세대 면역항암제를 개발해 온 넥타테라퓨틱스가 난관에 봉착했다. 올해 초 BMS와 총 계약금 4조원에 달하는 빅딜을 성사시켰던 신약후보물질 'NKTR-214'을 향해 시장가치가 '제로'라는 혹평이 제기되면서다.
거액을 들여 NKTR-214 개발권을 확보한 BMS는 물론, 비슷한 기전의 항암제를 개발 중인 국내 기업 제넥신을 향해서도 불확실성이 확산되는 것 아니냐는 우려가 나온다.
◆넥타 기대주 'NKTR-214' 비관론 대두…주가 급락
글로벌 투자컨설팅업체 플레인뷰(Plainview LLC)는 최신 보고서에서 "넥타가 개발 중인 지속형 인터루킨-2 'NKTR-214'의 시장 가치가 제로"라고 평가했다. 보고서에는 넥타의 기업가치를 수십억달러로 끌어올린 파이프라인의 성공가능성이 희박하다는 주장이 담겼다.
이 보고서는 이 같은 주장에 대해 다양한 근거를 제시한다.
IL-2가 임상반응을 나타내려면 림프구가 200~300% 가량 늘어야 하는데, 먼저 공개된 데이터에서 NKTR-214가 림프구를 33~55% 증가시키는 데 그쳤다는 게 그 중 하나다. 약물 성분이 체내 흡수되는 지표를 의미하는 혈중약물농도(AUC)를 따져볼 때, IL-2 자체값이 7~20%인 데 비해 페길레이션 형태인 NKTR-214의 최신 데이터는 7~11%에 그쳤다는 내용도 언급됐다. NKTR-214의 최고농도가 IL-2의 약 2%로, 장기간 지속되는 효능이 거의 없다는 지적이다.
지난 1일(현지시각) 시킹알파(Seeking Alpha) 등 다수 언론을 통해 관련 내용이 보도되자 넥타 주가는 큰 타격을 입었다. 지난주까지 60달러 전후에 거래되던 넥타사의 주가는 2일 오후 약 10% 떨어진 54.79달러까지 하락했다. 기대 이하의 반응률을 발표하면서 주가가 42% 떨어졌던 미국임상종양학회(ASCO 2018) 때와 비슷한 수준이다.
미국의 투자전문매체 시킹알파는 플레인뷰의 보고서를 인용하면서 "NKTR-214는 이미 단일요법 임상에서 반응률 0%를 기록했다. ASCO 2018 발표 데이터에 미뤄볼 때 옵디보 병용요법이 실패할 확률도 높아보인다"고 보도했다.
미국의 의약전문지 피어스파마(FiercePharma)는 NKTR-214의 항암치료 효과와 관련해 "400°F에 10분간 요리할 수 있는 스테이크를 4°F에 1000분 동안 가열하는 것과 같은 원리다. 종양세포를 죽일만큼 효과가 크지 않다는 의미"라고 설명했다.
◆ASCO 2018 발표 데이터, 반응률 급감…투자자 신뢰 잃어
NKTR-214 개발을 두고 처음부터 비관론이 제기됐던 건 아니다. NKTR-214는 재조합 인터루킨-2(IL-2)에 페길레이션(PEGylation) 기술을 접목한 CD122 작용제다. IL-2 신호전달과정을 타깃해 종양침투림프구(TIL)의 비율을 높이는 기전을 갖는다. 넥타는 페길화된 IL-2가 반감기를 연장하고, 조절T세포(Treg)의 증식을 유도하는 IL2Rαβγ와의 상호작용을 차단할 수 있다는 가정 아래 NKTR-214 개발에 박차를 가해왔다.
올해 초 BMS와 기술수출 계약을 체결할 당시만 해도 NKTR-214는 차세대 인터루킨 시장의 선두주자로 기대를 받았다.
지난 2월 BMS가 NKTR-214를 면역관문억제제 '옵디보(니볼루맙), 여보이(이필루맙)'와 병용 치료제로 개발하는 대가로 보장한 금액은 최대 36억달러(4조320억원)에 달한다. BMS는 선계약금 10억달러를 지불하는 동시에 넥타 주가에 36%의 프리미엄을 더한 8억5000만달러의 주식을 사들이고, 추가 마일스톤으로 18억달러를 약속했다. 흑색종, 신세포암, 비소세포폐암, 방광암, 삼중음성유방암 등 9개 암종에서 20여 개 적응증에 대해 NKTR-214와 옵디보 병용요법의 효능을 평가한다는 조건이다.
옵디보뿐 아니라 아스트라제네카의 '티센트릭(아테졸리주맙)'이나 MSD의 '키트루다(펨브롤리주맙)'와의 병용 가능성을 평가하기 위한 임상도 진행되고 있다. 넥타 테라퓨틱스 주가가 최근 1년새 약 3배 증가했다는 사실은 NKTR-214 개발 성공에 대한 기대치를 방증한다.
지난해까지 NKTR-214가 면역관문억제제와의 병용을 통해 보여준 효능은 놀라웠다. SITC 2017에서 발표된 PIVOT 1/2상임상 결과, NKTR-214와 옵디보 병용 시 ORR은 64~75%, 질병조절률(DCR)은 75~91%에 달했다. 흑색종(11명)과 신세포암(14명) 환자의 ORR은 각각 64%와 57%였다.

그런데 넥타는 기술수출 4개월 여만인 ASCO 2018 대회부터 투자들의 신뢰를 잃기 시작한다.
이 회사는 '임상연구에 참여한 피험자 283명 중 87명(31%)이 반응했다'는 제한된 정보만을 공개했다. 1, 2기 흑색종과 신세포암 환자 전체의 반응률 발표를 미룬 채, 2기 환자의 반응률만 발표한 것이다. 당시 흑색종과 신세포암 환자의 반응률은 SITC 2017 때보다 크게 떨어진 20%(3/15명)와 33%(5/15명)에 그쳤다.
시킹알파는 "투자자들은 바이오기업이 임상 결과 발표를 보류할 때 항상 데이터가 예상보다 나빴다는 사실을 기억해야 한다. 반응률이 급감했다는 사실을 감추려는 의도로 판단된다"며 "올해 면역항암학회(SITC 2018)에서 공개될 추가 데이터에서도 반응률이 개선될 확률은 희박하다"고 언급했다.
애론 웰룬(Aaron Wedlund) 애널리스트는 "지난 1년간 넥타의 주가를 3배나 끌어올린 NKTR-214 개발은 실패할 것이다. 키트루다와 병용임상을 시도하다 중단됐던 인사이트의 에파카도스타트(epacadostat)의 뒤를 잇게 될 것"이라고 전했다.
◆BMS·제넥신에도 여파…11월 SITC 학회 발표가 변수
시장의 우려는 비단 넥타테라퓨틱스 한 기업에 그치지 않는다. NKTR-214와 옵디보 병용요법에 큰 기대를 걸어온 BMS를 향해 불안심리가 확산되고 있다.
미국의 의약전문지 피어스파마는 "NTKR-214 개발실패가 현실화 할 경우 거액을 투자해 NKTR-214 개발권리를 확보한 BMS에게도 파장이 예상된다. 비소세포폐암 1차치료제 임상 실패로 한차례 타격을 입었던 BMS는 이미 전체 계약금 36억달러 중 10억달러를 선지급했다"며 "ASCO 2018 당시 병용기간이 짧아 반응률이 낮게 나왔다고 해명했지만 3상임상까지 진행할 수 있을지 의문이다"라고 평가했다.
NKTR-214의 성패는 국내 기업 제넥신에 대한 시장 평가와도 상당한 연관성을 갖는다. 제넥신은 인터루킨-7(IL-7)에 자체 개발한 지속형 플랫폼기술을 접목한 항암신약 하이루킨-7(Hyleukin-7)을 개발 중이다. NKTR-214과 개발원리가 유사한 탓에 넥타와는 글로벌 피어그룹으로 평가된다. 실제 지난 6월에는 넥타의 NKTR-214 반응률이 급감했다는 소식이 전해지면서 주가가 동반하락한 전력이 있다.
NKTR-214의 반응률이 나아질 기미가 보이지 않는다면 글로벌 기술수출 기대감을 키우고 있는 제넥신의 하이루킨-7을 향한 불확실성마저 높아질 수 있다는 분석이 제기된다.
다음달 발표를 앞둔 하이루킨-7의 임상 결과는 제넥신에 대한 해외 시장평가의 중요한 변수다. 제넥신은 11월 7~11일 개최되는 SITC 2018 학회에서 고형암 환자 대상으로 하이루킨-7의 투여반응을 평가한 1b상임상 결과를 발표한다고 알려졌다.
선민정 하나금융투자 연구원은 최근 보고서에서 "넥타사가 SITC 학회에서 NTKR-214의 추가 임상 결과를 발표한다. 제넥신도 하이루킨-7이 암환자에게 정상인과 동일한 T세포 증가를 나타내는지 확인할 수 있는 1b상임상 결과를 처음 공개한다"며 "암환자 대상의 하이루킨 임상 데이터가 처음 공개되는 자리라는 점에서 중요한 의미를 가질 수 있을 것으로 기대된다"고 전했다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| [마켓인]네오이뮨텍, 프리IPO로 1500억 투자유치 나선다 (0) | 2018.10.10 |
|---|---|
| [기고]2018년 노벨 생리의학상 수상의 시사점 (0) | 2018.10.10 |
| "제넥신, 11월 면역항암제 학회 후 R&D 모멘텀 주목" (0) | 2018.10.01 |
| "글로벌 전문가 모셔라"…바이오 업체 잇단 영입 (0) | 2018.09.29 |
| 제넥신 "지속형 성장호르몬 2상, 12개월서도 효과 확인" (0) | 2018.09.28 |
글
http://view.asiae.co.kr/news/view.htm?idxno=2018100106190813768
![[클릭 e종목]"제넥신, 11월 면역항암제 학회 후 R&D 모멘텀 주목"](http://cphoto.asiae.co.kr/listimglink/1/2018100106184026212_1538342321.jpg)
[아시아경제 문채석 기자]하나금융투자는 1일 제넥신
에 대해 다음달 열릴 면역항암제 학회에서 발표할 하이루킨7의 임상1b 결과에 주목하라고 조언했다. 투자의견 '매수', 목표주가 15만원을 유지했고 직전 거래일인 지난달 28일 종가는 10만4000원이다.
선민정 하나금융투자 연구원은 지난 6월 미국임상종양학회(ASCO)에서 제넥신과 같은 업계의 글로벌 기업 넥타(Nektar Therapeutics)사가 지속형 IL-2-옵디보(면역관문억제제) 병용투여 임상 결과 기존 대비 객관적 반응률(ORR·Objective Response Rate)이 적게 나오며 주가가 42% 빠졌고 제넥신도 다음날 동반 하락한 바 있다고 설명했다.
선 연구원은 당시 ASCO 임상 2상 결과는 초기 데이터에 불과하며 ORR도 회복될 것으로 봤다. 본 게임은 다음달 7일 열리는 면역항암제 학회(SITC)라는 시각이다. 넥타사도 ASCO 이후 데이터를 발표, ORR이 늘어났음을 증명할 것으로 보이고 제넥신도 같은 학회에서 하이루킨 7(HyLeukin-7)의 임상1b상 결과를 발표한다.
선 연구원은 "고형암 대상 하이루킨-7 투여시 정상인에게서 나타났던 반응인 6개월 T세포 숫자 증가 반응이 나타나는지 확인해보는 임상으로 암환자 대상으로 처음 공개하는 결과"라며 "다음달 SITC에 이어 내년부터 본격적으로 하이루킨-7의 임상결과들이 공개될 것으로 예상돼 제넥신의 연구·개발(R&D) 관련 성장 동력(모멘텀)은 쭉 커질 것"이라고 봤다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| [기고]2018년 노벨 생리의학상 수상의 시사점 (0) | 2018.10.10 |
|---|---|
| 넥타 '인터루킨 면역항암제' 실패설…불안심리 확산 (0) | 2018.10.05 |
| "글로벌 전문가 모셔라"…바이오 업체 잇단 영입 (0) | 2018.09.29 |
| 제넥신 "지속형 성장호르몬 2상, 12개월서도 효과 확인" (0) | 2018.09.28 |
| 면역항암제 병용투여 강력후보 제넥신 하이루킨 기대↑ (0) | 2018.09.23 |
글
http://www.newspim.com/news/view/20180928000219
바이오 업체들이 잇따라 글로벌 전문가들을 영입하고 있다. 해외 시장이 중요해지고, 임상 단계가 진행되며 기술이전의 가능성이 커지자 관련 전문가들을 수혈하는 것이다.
 |
| [사진=게티이미지뱅크] |
29일 관련 업계에 따르면 제넥신은 최근 김광호 전 존슨앤드존슨(J&J) 북아시아 총괄사장을 부사장으로 영입했다. 김 부사장은 제넥신에서 최고운영책임자(COO)로서 경영 부문을 총괄할 계획이다.
제넥신 관계자는 "신약후보물질(파이프라인)들이 늘어나고, 임상 단계가 진행됨에 따라 경영 부문의 전문성을 강화해야겠다고 판단했다"고 "제넥신이 세계적 기업으로 도약하는데 김 부사장의 다국적 기업 경영 경험이 도움이 될 것"이라고 말했다.
제넥신은 약효를 길게 지속시키는 기반기술인 하이브리드FC(HyFc)를 이용해 지속형 성장호르몬 등을 개발하고 있다. 5개의 파이프라인이 임상 2상 단계에 있다. 통상적으로 신약후보 물질 가치가 높아지는 임상 2상부터 기술이전이 일어난다.
바이오 벤처기업 올릭스도 이달 미국 보스턴 바이오메디컬 출신 웨이 리(Wei Li) 씨를 최고개발책임자(CDO)로 영입했다.
리 CDO는 미국 보스턴 바이오메디컬에 2007년 사업개발 책임자로 입사 후, 기술개발부터 임상개발 분야를 총괄했다. 2012년 일본 스미토모 다이니폰 제약이 보스턴 바이오메디컬을 약 26억달러(약 2조9000억원)에 인수할 당시에는 이를 담당한 바 있다.
리 CDO는 올릭스의 사업개발 및 기술이전 등을 담당할 예정이다. 다음 달 미국 보스턴 지역에 설립될 올릭스의 미국 지사를 총괄한다.
에이티젠은 미국 스템셀, 스템메디카 셀 테크놀로지 등 바이오 기업에서 의약품 제조관리(GMP) 기준 업무를 40년 이상 수행한 케너스 버거 박사를 영입했다. 메디프론은 미국 바이오 기업 셀로믹스, SCM 생명과학, 지플러스 생명과학 등에서 신약 개발을 주도한 유영동 박사를 중앙연구소장으로 선임했다.
바이오 기업들이 이처럼 글로벌 전문가 영입에 나선 것은 해외 시장과 기술이전의 중요성이 커졌기 때문이다.
임상시험의 경우 단계가 진행될수록 비용이 늘어난다. 특히 대규모 임상을 해야 하는 임상 3상의 경우 막대한 자금이 들기 때문에 국내 바이오 벤처기업이 진행하기 어렵다. 이 때문에 기술이전이 필수적이다.
바이오 업계 관계자는 "해외 기술이전을 하기 위해서는 다국적 제약사들의 수요를 파악해야 하고, 네트워크도 형성해야 한다"며 "바이오 벤처기업들이 이를 위해 글로벌 전문가들을 데려오는 것"이라고 설명했다.
업계에서는 바이오 벤처 기업들이 성숙해지고, 주요 파이프라인들의 임상 단계가 진행되고 있는 만큼 글로벌 전문가 영입이 더 늘어날 것이라고 내다봤다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| 넥타 '인터루킨 면역항암제' 실패설…불안심리 확산 (0) | 2018.10.05 |
|---|---|
| "제넥신, 11월 면역항암제 학회 후 R&D 모멘텀 주목" (0) | 2018.10.01 |
| 제넥신 "지속형 성장호르몬 2상, 12개월서도 효과 확인" (0) | 2018.09.28 |
| 면역항암제 병용투여 강력후보 제넥신 하이루킨 기대↑ (0) | 2018.09.23 |
| 제넥신, CPA 전처리 후 면역항암제 투여 1b상 진입 (0) | 2018.09.21 |
글
http://biospectator.com/view/news_view.php?varAtcId=6275
키 성장속도 분석결과 유럽 소아내분비학회 발표..지노트로핀 대비 주 1회(0.8mg/kg, 1.2mg/kg)/2주 1회(2.4mg/kg) 모두 우수한 결과..내년 상반기 美 3상 신청 예정

제넥신이 소아 환자 대상 GX-H9의 임상 2상 12개월 결과분석을 통해 지속형 성장호르몬의 가능성을 확인했다. GX-H9은 제넥신의 원천기술인 hyFcTM(hybrid Fc) 를 적용한 주 1회 또는 월 2회 투여를 목표로 한독과 공동 개발중인 지속형 성장호르몬이다. 내년 상반기 미국 3상 승인신청서 제출을 준비중이다.
제넥신은 27일(현지시간) 그리스에서 열린 제 57회 유럽 소아내분비학회(The 57th Annual ESPE Meeting)에서 지속형 성장호르몬 GX-H9의 소아 환자를 대상으로 유럽/한국에서 진행한 임상 2상의 12개월 키 성장속도 결과를 발표했다.
제넥신은 현재 유럽 및 한국 10개국 27개의 내분비센터에서 연장연구 진행 중인 소아 임상 2상의 12 개월 치료를 완료한 50명의 환자를 대상으로 일일 제형인 지노트로핀(Genotropin®)과 GX-H9의 12개월 키 성장속도를 비교했다.
공개된 자료에 따르면 지노트로핀을 매일 투여한 대조군의 연간 키 성장속도는 약 9.14cm/년인 반면 GX-H9를 주 1회 간격으로 0.8mg/kg 투여한 군과 1.2mg/kg 투여한 군은 각각 약 10.50cm/년과 약 11.76cm/년의 성장속도를 보였다. 2주 1회 간격으로 2.4mg/kg을 투여한 군은 약 11.03cm/년의 키 성장속도를 보이며 대조군과 비교해 우수한 결과를 나타냈다.
제넥신은 임상 2상 6개월 결과에서도 비슷한 결과를 얻었다. 지노트로핀 매일 투여군은 연간 키 성장속도가 11.24cm/년인 반면 GX-H9를 주 1회 간격으로 0.8mg/kg 투여한 군과 1.2mg/kg 투여한 군은 각각 11.50cm/년, 11.54cm/년을 기록했다. 또한 2주 1회 간격으로 2.4mg/kg을 투여한 군 역시 11.86cm/년이었다.
이번에 발표된 12개월 결과는 6개월 결과와 비교 시, 유의미한 키 성장속도의 둔화가 관찰되지 않았고 현재까지 주사 부위의 지방위축증, 인슐린 저항성 등의 부작용이 보고되지 않아 지노트로핀 투약군과 동등한 수준의 안전성을 보였다. 특히 주 1회 및 2주 1회 용법으로 투여 시, 모두 대조군과 비교해 우수한 키 성장속도를 보이며 주 1회뿐 아니라 월 2회 지속형 제형으로서의 가능성을 확인했다는게 회사측의 설명이다.
한편 GX-H9는 글로벌 신약개발 R&D를 지원하는 범부처신약개발사업단의 범부처전주기신약개발사업 과제로 선정돼 ‘차세대 인성장호르몬 제제 (GX-H9)의 소아 성장호르몬 결핍 환자 (PGHD) 대상 글로벌 임상 2상 승인 및 수행, 글로벌 라이센스 아웃’ 연구를 성공적으로 진행하고 있다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| "제넥신, 11월 면역항암제 학회 후 R&D 모멘텀 주목" (0) | 2018.10.01 |
|---|---|
| "글로벌 전문가 모셔라"…바이오 업체 잇단 영입 (0) | 2018.09.29 |
| 면역항암제 병용투여 강력후보 제넥신 하이루킨 기대↑ (0) | 2018.09.23 |
| 제넥신, CPA 전처리 후 면역항암제 투여 1b상 진입 (0) | 2018.09.21 |
| 펀드매니저와 애널의 제약·바이오 투자팁..."고릴라 게임+임상후 상용화 고려" (0) | 2018.09.20 |
글
http://www.docdocdoc.co.kr/news/articleView.html?idxno=1060716
면역항암제에 대한 병용 임상 연구가 활발해지면서 제넥신의 면역항암제 하이루킨-7에 대한 기대도 덩달아 높아지고 있다.
식품의약품안전처는 지난 20일 전이성, 재발성 고형암 환자를 대상으로 한 하이루킨-7의 병용투여 임상을 승인했다.
병용 투여는 화학적 항암요법제인 ‘CPA(사이클로포스파마이드, Cyclophosphamide)’를 전처리 한 후 하이루킨-7 투여가 이뤄지는 형태다.
이번 임상은 서울대병원에서 고형암 환자를 대상으로 2년간 1b상(안전성과 내약성 등 평가)과 2a상(객관적 반응률과 생존기간 평가)이 순차적으로 진행될 예정이다.
제넥신에 따르면 하이루킨-7 단독투여시 항암에 관여하는 항체 증가 및 암세포를 파괴하는 종양침윤세포(TILs)가 증가하는 것으로 나타났다. CPA와 병용투여시에는 T세포가 크게 증가하고 시너지 효과로 높아진 항종양 효과가 있다는 게 회사의 설명이다.
고형암과 뇌암을 대상으로 한 하이루킨-7 단독투여 임상은 국내서 진행 중이다.
이와 함께 유방암을 대상으로 키트루다(성분명 펨브롤리주맙)와의 하이루킨-7 병용 임상(1b, 2a)도 대기 중에 있다.
제넥신은 범부처신약개발사업단(KDDF) 과제로 선정된 이 연구에 대한 IND(임상시험계획승인신청)를 연내 제출하겠다는 계획이다.
제넥신 관계자는 “키트루다와의 유방암 병용 임상은 올해 11월내로 식약처에 IND를 제출하려고 한다”면서 “이후 환자모집을 통해 임상이 이뤄질 것”이라고 설명했다.
한편 증권가에선 이같은 병용투여에 대한 기대감과 임상 성공확률을 추정해 하이루킨-7의 가치가 1조원대에 이른다고 분석하기도 했다.
KTB투자증권 강하영 연구원은 하이루킨을 면역항암제와의 병용투여가 가장 기대되는 약물로 꼽고, 현재(2018년 4월 기준)가치를 9,162억원이라고 판단했다.
강 연구원은 “하이루킨-7의 체내 안정성을 감안해 신약개발 성공률을 15%로 산정했다”면서 “면역항암제의 가장 큰 단점이 낮은 반응률인 만큼 글로벌제약사들도 반응률을 높이기 위해 다른 면역항암제나 케미컬 항암제 등을 병용투여 하는 임상을 활발히 하고 있는 상황”이라고 설명했다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| "글로벌 전문가 모셔라"…바이오 업체 잇단 영입 (0) | 2018.09.29 |
|---|---|
| 제넥신 "지속형 성장호르몬 2상, 12개월서도 효과 확인" (0) | 2018.09.28 |
| 제넥신, CPA 전처리 후 면역항암제 투여 1b상 진입 (0) | 2018.09.21 |
| 펀드매니저와 애널의 제약·바이오 투자팁..."고릴라 게임+임상후 상용화 고려" (0) | 2018.09.20 |
| 제넥신, 지속형 성장호르몬 소아 임상 2상 결과 발표 예정 (0) | 2018.09.14 |
글
http://m.medipana.com/news_viewer.asp?NewsNum=225696&MainKind=C&NewsKind=67&vCount=4&vKind=1
CPA는 림프종, 기관지암, 자궁경부암 등에 널리 사용되는 세포독성 알킬화약물로 단독 또는 다른 항암제와 복합해 사용하는 화학적 항암제다.
'바이오종목 > 제넥신' 카테고리의 다른 글
| 제넥신 "지속형 성장호르몬 2상, 12개월서도 효과 확인" (0) | 2018.09.28 |
|---|---|
| 면역항암제 병용투여 강력후보 제넥신 하이루킨 기대↑ (0) | 2018.09.23 |
| 펀드매니저와 애널의 제약·바이오 투자팁..."고릴라 게임+임상후 상용화 고려" (0) | 2018.09.20 |
| 제넥신, 지속형 성장호르몬 소아 임상 2상 결과 발표 예정 (0) | 2018.09.14 |
| "세계 최초 hyFc 플랫폼·DNA 백신 개발 멀지 않았다" (0) | 2018.09.12 |


RECENT COMMENT