검색결과 리스트
글
CAR-T 치료제 ‘킴리아’는 어떻게 개발에 성공했나 미충족 수요 반영한 FDA 도움 및 관해율 ‘눈길’…한계점도 존재
설정
트랙백
댓글
http://www.yakup.com/news/index.html?mode=view&pmode=&cat=12&cat2=&cat3=&nid=225604&num_start=0
=====================================================================
세계 최초의 CAR-T 세포 유전자치료제인 킴리아(성분명: 티사젠렉류셀)의 개발 성공 요인은 미국 FDA 등의 신속한 승인 및 대응, 지속적인 정부 연구비 지원, 암 환자의 시급한 미충족 수요(Unmet Need), 높은 관해율 등인 것으로 나타났다.
그러나 개발 저해 요인으로는 제조공정이 복잡하고 대량생산이 불가능해 나타난 비용의 상승, 비표적 부작용, 고형암에 대한 낮은 치료 가능성 등이 존재하는 것으로 나타났다.
글로벌 첨단바이오의약품 코디네이팅센터(CoGiB)는 과학기술정보통신부․보건복지부 사업의 일환으로 시행한 ‘2018 킴리아 성공요인 분석보고서’를 최근 발표하고 이같이 밝혔다.
킴리아는 2012년 8월 암 치료를 위한 CAR-T 개발을 목표로 노바티스와 펜실베이니아 대학교(UPenn)가 연구공동체를 설립해 개발한 치료제다.
항암제의 경우, 임상의 평가변수가 생존율을 기반으로 하기 때문에 추적 관찰 기간을 포함하는 임상기간이 매우 긴 것이 특징이다. 그러나 킴리아의 경우 임상기간이 약 5년으로 확인됐다.
이는 1980년대 중반부터 정부 연구비의 지원을 받아 T 세포의 적응면역(Adoptive Immune) 치료제 임상연구의 기반을 다져놓았기 때문에 그만큼의 데이터들이 축적돼 있기 때문이라고 보고서는 전했다.
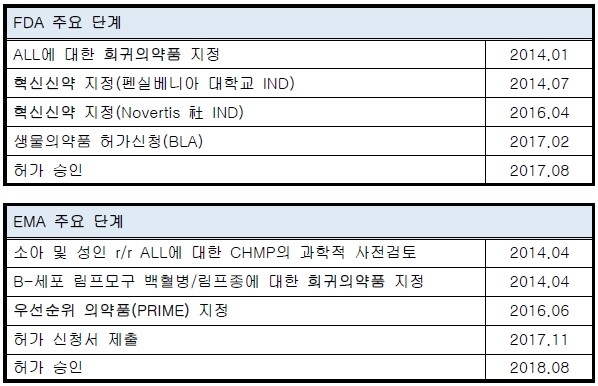
킴리아의 개발 성공에는 미국 FDA의 신속한 승인 및 대응도 한 몫 했다. 킴리아는 FDA에서 신속 승인절차로 허가를 받을 수 있는 혁신 치료제(Breakthrough Therapy)로 지정되면서 조기에 시장에 진출할 수 있었다.
또 CAR-T 세포 치료제의 특성상 킴리아는 기존 치료법으로 실패한 전이암, 재발암에 대한 치료 효과가 높아 현재 시급하게 해결되어야 할 암환자의 미충족 의료 수요(Unmet Medical Needs)에 걸맞게 개발됐다는 분석이다.
FDA에서는 이러한 점을 감안해 CAR-T 세포 치료제의 임상시험 중 사망자 발생에 대한 보고에도 임상시험을 중단시키지 않거나, 보류 조치 후 빠른 재개 허용 등의 조치를 내린 바 있다. 임상시험 중 발생한 사망사고로 인해 시험이 중단될 시 해당 원인 조사에는 보통 8개월이 소요된다.
킴리아는 글로벌 2상 임상시험(ELIANA)의 중간 평가에서, 투여 환자의 81%가 완전 관해(60%) 또는 불완전한 혈액학적 복구를 동반한 완전관해(21%)에 도달했으며, 이들 환자의 1년 생존율은 76%, 50%는 치료 12개월 후에도 재발이 없는 것을 확인했다.
그러나 한계점도 여실히 드러났다. 환자 개인맞춤형으로 제조되는 자가 CAR-T 세포 치료제는 제조과정이 복잡하고 대량생산이 불가해 비용이 많이 소모되고 불확실성이 높아지는 단점이 있는 것.
제조공정으로 인한 CAR-T 세포 치료제의 고비용으로 킴리아는 약값만 한화 약 5억 2천만원(475,000달러)에 달하며, 부대비용까지 더할 경우 약값이 천정부지로 높아진다.
또 킴리아의 주된 부작용으로 사이토카인 방출 증후군(Cytokine Release Syndrom, CRS)과 신경독성(Neurotoxicity)이 존재하는 것으로 나타났다.
킴리아와 같은 항 CD19 CAR-T 세포 치료제는 암 세포뿐만 아니라 CD19를 발현하고 있는 정상세포도 파괴한다. 항 CD19 CAR-T 세포 치료제에 대한 두 종류의 재발도 일어나 환자의 20~50%가 재발한다는 통계도 있다.
특히 백혈병 세포 위의 CD19가 소실되거나 하향 조절되며 재발되는 CD19-음성 재발에 대해서는 대안적인 CAR-T 세포 유전자치료도 효과가 없고 유지도 불가능하기 때문에 특히 우려된다고 보고서는 밝혔다.
또 CAR-T 세포 치료제는 현재로서는 그 효능이 고형암에서 매우 제한적인 상황이다. 이와 관련해 연구 개발이 활발하게 전개되고 있지만, 언제쯤 가시적인 성과가 나타날지는 미지수다.
보고서는 “CAR-T 세포 치료제는 새로운 치료법이기 때문에 작용기전, 안전성, 재발여부 등 임상 데이터가 충분히 확보되지 못한 점이 넘어야 할 관문”이라며 “그럼에도 불구하고 다양한 암 치료제로서의 활용 가능성, 혁신적 신약으로서 인정, 큰 경제적 파급효과 등이 시장의 기회요인으로 작용할 것”이라고 전망했다.
'경제뉴스' 카테고리의 다른 글
| 유전자치료 (0) | 2018.12.23 |
|---|---|
| 실현가능한 R&D과제 자산화 가능...금감원, 점검 착수 (0) | 2018.12.21 |
| '항암제 세대교체' 면역항암제 6인방 성적표는? (0) | 2018.12.10 |
| DPP-4i 성장둔화 속 국내 제약사 약진 '주목' (0) | 2018.12.10 |
| 급성장중인 중국 제약 시장‥적극적 개편과 투자가 이유 (0) | 2018.12.08 |


RECENT COMMENT